有一包白色固体可能含碳酸钠、硫酸钠、氯化钠、硝酸钡、氢氧化钾中的一种或几种。某科学兴趣小组按以下操作检测其成分:
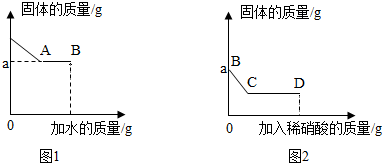
I.取少量固体于烧杯中,逐渐加水并不断搅拌,烧杯内固体的质量随加入水的质量的变化如图1;
Ⅱ.继续向烧杯中滴加稀硝酸并不断搅拌,烧杯内固体的质量随加入稀硝酸的质量的变化如图2所示。
请回答下列问题:
(1)图2中BC段可观察到的现象是 固体部分溶解,有气泡冒出固体部分溶解,有气泡冒出;
从C到D的过程中,液体的pH将逐渐 减小减小(填“增大”、“减小”或“不变”);
到达D点时,溶液中含有的溶质有 三三种(填“—”、“二”或“三”)。
(2)原白色固体中一定含有的物质是:碳酸钠、硫酸钠、硝酸钡碳酸钠、硫酸钠、硝酸钡。
【答案】固体部分溶解,有气泡冒出;减小;三;碳酸钠、硫酸钠、硝酸钡
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/18 3:0:2组卷:7引用:1难度:0.5
相似题
-
1.某混合气体X由CO2、CO、H2O(水蒸气)、H2中的两种或两种以上组成,X气体依次通过如图1装置(假定每步反应均完全),现象分别为:A中溶液变浑浊;B中固体变为红色;C中粉末变为蓝色;D中溶液变浑浊。
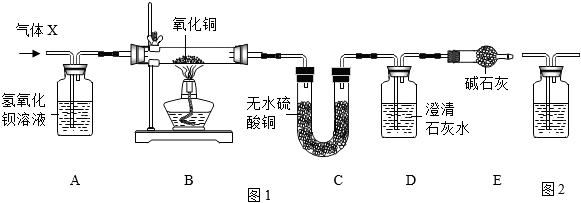
完成下列问题:
(1)该实验能得出CO气体一定存在的证据是;
(2)只要在图1中加装一个图2装置,就能确定原混合气体X中是否含有H2。
①写出图2装置中试剂名称;
②该装置连接在图1中哪两个装置之间(用字母表示)。发布:2024/12/28 16:0:2组卷:208引用:8难度:0.5 -
2.碱式碳酸锌[Znx(OH)y(CO3)Z]是制备ZnO的原料,其化学反应表达式为:Znx(OH)y(CO3)Z
ZnO+CO2↑+H2O(x,y,z为正整数)。小金设计了图甲所示装置对碱式碳酸锌的组成进行探究(装置气密性良好,药品足量,实验操作正确):熔烧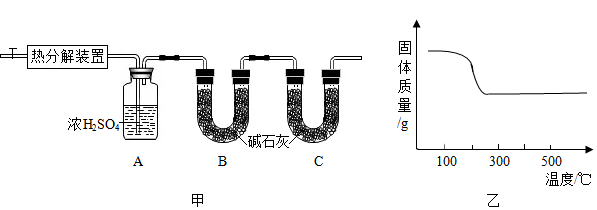
(1)图甲中装置B的作用是。
(2)查阅资料发现,在不同温度条件下充分加热等质量的碱式碳酸锌样品,剩余固体的质量与加热温度的关系如图乙所示。实验中加热时,热分解装置的温度至少要达到℃(选填“200”“300”或“400“),才能彻底分解碱式碳酸锌。
(3)部分实验步骤为:“⋯⋯加热前先通入N2排尽装置内的空气,关闭通入N2的活塞,⋯⋯控制一定温度下加热⋯⋯”。实验过程中,可根据哪一装置中的什么现象来判断碱式碳酸锌样品已完全分解?发布:2024/12/28 16:30:2组卷:33引用:2难度:0.5 -
3.工业上用电解饱和食盐水的方法制备烧碱,小乐对用此方法生产的、外包装破损的烧碱样品进行了如下探究。
【提出问题】烧碱样品中含有哪些杂质?
【建立猜想】猜想1:可能含有碳酸钠,依据是氢氧化钠能和二氧化碳反应生成碳酸钠。
猜想2:可能含有氯化钠,依据是在化工生产中,原料可能。
【实验探究】
【反思评价】除去烧碱样品中含有的少量碳酸钠,可选用的药品是实验操作 实验现象 实验结论 取少量烧碱样品于试管中,加适量水溶解,加入过量的稀硝酸,再滴加少量硝酸银溶液 烧碱样品中含碳酸钠和氯化钠 。
A.CuCl2溶液
B.Ba(NO3)2溶液
C.Ba(OH)2溶液
D.KOH溶液发布:2024/12/28 16:0:2组卷:22引用:9难度:0.5


