高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中湿法制备高铁酸钠的原理为:3NaClO+2Fe(OH)3+4NaOH═2Na2FeO4+3NaCl+5H2O。
(1)高铁酸根(FeO2-4)中铁元素的化合价为 +6+6;该反应中氧化剂是 NaClONaClO;被氧化的元素是 铁元素铁元素(填名称);氧化产物是 Na2FeO4Na2FeO4。
(2)请用双线桥表示该氧化还原反应中电子转移的方向和数目: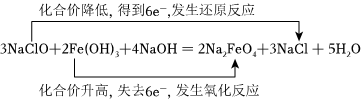
 。
。
(3)若有0.15mol次氯酸钠参加反应,则转移的电子数为 0.3NA0.3NA,生成 0.10.1molNa2FeO4。
(4)写出湿法制备高铁酸钠的离子方程式:3ClO-+4OH-+2Fe(OH)3=2FeO2-4+3Cl-+5H2O3ClO-+4OH-+2Fe(OH)3=2FeO2-4+3Cl-+5H2O。
F
e
O
2
-
4


F
e
O
2
-
4
F
e
O
2
-
4
【答案】+6;NaClO;铁元素;Na2FeO4; ;0.3NA;0.1;3ClO-+4OH-+2Fe(OH)3=2+3Cl-+5H2O
;0.3NA;0.1;3ClO-+4OH-+2Fe(OH)3=2+3Cl-+5H2O
 ;0.3NA;0.1;3ClO-+4OH-+2Fe(OH)3=2
;0.3NA;0.1;3ClO-+4OH-+2Fe(OH)3=2F
e
O
2
-
4
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/8/6 8:0:9组卷:8引用:2难度:0.5
相似题
-
1.根据下列两个反应判断:2Cu+O2=2CuO,2Cu+S=Cu2S,下列叙述中错误的是( )
发布:2024/12/30 14:30:1组卷:16引用:2难度:0.9 -
2.将适量的SO2通入Fe(NO3)3溶液中,溶液逐渐由棕黄色变为浅绿色,但又立即变为棕黄色,继续滴入BaCl2溶液,产生白色沉淀。在上述一系列变化过程中,最终被还原的元素是( )
发布:2024/12/30 14:30:1组卷:27引用:2难度:0.6 -
3.实验证明,在一定温度和压强下,用铜的化合物做催化剂,甲烷(CH4)与氧气反应只生成甲醇(CH3OH)。下列叙述正确的是( )
发布:2025/1/7 8:0:2组卷:2引用:1难度:0.7


