我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献。如图为联合制碱法的主要过程(部分物质已略去)
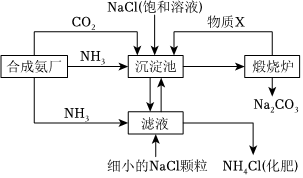
已知:i.NH3溶于水生成碱,与酸反应生成盐,如NH3+HNO3=NH4NO3
ⅱ.有关物质的溶解度如下表:
| 物质 | NaCl | NH4HCO3 | NaHCO3 | NH4Cl |
| 20℃溶解度/g | 36.0 | 21.7 | 9.6 | 37.2 |
(1)“沉淀池”中发生了化合反应和复分解反应,其化学方程式为:NH3+CO2+H2O=NH4HCO3、
NH4HCO3+NaCl=NaHCO3↓+NH4Cl
NH4HCO3+NaCl=NaHCO3↓+NH4Cl
。(2)下列说法正确的是
AC
AC
(填序号字母)。A.“沉淀池”中有NaHCO3析出,因为该条件下NaHCO3的溶解度最小
B.“滤液”中主要含有NaCl、Na2CO3和NH4Cl
C.设计循环的目的是提高原料的利用率
(3)“煅烧炉”中发生的是分解反应,化学方程式为
2NaHCO3
Na2CO3+CO2↑+H2O
Δ |
2NaHCO3
Na2CO3+CO2↑+H2O
物质X是 Δ |
CO2
CO2
(填化学式)。(4)某小组同学探究Na2CO3与盐酸的反应。取1.06gNa2CO3固体加水溶解后,配成100mL溶液,则Na2CO3的物质的量浓度为
0.1mol/L
0.1mol/L
;向其中滴加稀盐酸,开始无气泡,继续滴加,产生气泡,反应的离子方程式为:CO
2
-
3
HCO
-
3
HC
O
-
3
HC
O
-
3
【考点】纯碱工业(侯氏制碱法).
【答案】NH4HCO3+NaCl=NaHCO3↓+NH4Cl;AC;2NaHCO3
Na2CO3+CO2↑+H2O;CO2;0.1mol/L;+H+=CO2↑+H2O
Δ |
HC
O
-
3
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/9/27 2:0:1组卷:20引用:3难度:0.7
相似题
-
1.以NaCl为原料,可制取纯碱。Na2CO3可用侯氏制碱法制取,主要涉及如下反应:NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl;2NaHCO3
Na2CO3+CO2↑+H2O,下列有关实验室模拟侯氏制碱法的实验原理和装置正确的是( )△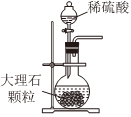
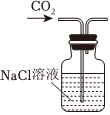
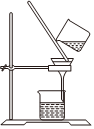
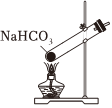
A.制取CO2 B.制取NaHCO3 C.分离NaHCO3 D.制取Na2CO3 发布:2024/12/8 18:0:1组卷:169引用:5难度:0.8 -
2.“侯氏制碱法”的主要过程如图(部分物质已略去)。
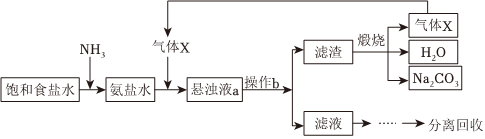
下列说法错误的是( )发布:2024/12/8 0:0:1组卷:135引用:4难度:0.7 -
3.氨碱法(索氏)和联合制碱法(侯氏)是两大重要的工业制碱法,下列表达正确的是( )
氨碱法 联合制碱法 A 原料 食盐、氨气、生石灰 食盐、氨气、二氧化碳 B 副产物 氯化钙 氯化铵 C 循环物质 氨气、二氧化碳 氯化钠 D 评价 原料易得、设备简单、能耗低 原料利用率高、废弃物少 发布:2024/12/16 6:0:1组卷:38引用:2难度:0.8


