绣绣要测定某大理石样品中碳酸钙的质量分数,她取一定质量的大理石磨成粉末与稀盐酸反应测量生成的二氧化碳的质量来完成实验,她采用了两个方案分别进行实验如下(实验中不考虑盐酸挥发、水的蒸发,杂质不参与化学反应):
【方案一】根据质量守恒定律获取二氧化碳质量
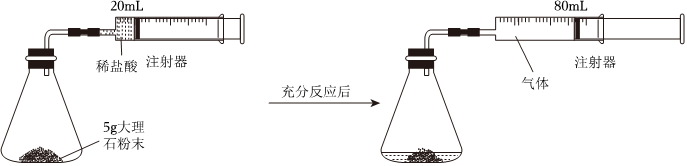
如图一,将5g大理石粉末放入锥形瓶中,分液漏斗中加入足量的稀盐酸,置于电子天平称出装置总质量,打开活塞,滴入足量稀盐酸后关闭活塞,将天平示数随反应时间变化的关系绘成图像如图二。

【方案二】根据收集的二氧化碳的体积获取二氧化碳质量
采用如图装置,先检测装置气密性,然后将5g大理石粉末置于锥形瓶中,将20mL稀盐酸迅速推入锥形瓶中,充分反应后,针筒活塞移动到80mL位置,如图所示。
(1)根据方案一计算大理石样品中碳酸钙的质量分数。
(已知:CaCO3+2HCl═CaCl2+CO2↑+H2O)
(2)方案二中,在检查装置气密性时,绣绣用双手捧住锥形瓶容器一段时间后再放开,若出现 注射器活塞先是向右移动一段距离,最后又回到原位置注射器活塞先是向右移动一段距离,最后又回到原位置的现象,则证明气密性良好。
(3)针对方案二,下列分析正确的有 CC。
A.注射器中收集到的是纯净的CO2气体
B.共生成了80mLCO2气体
C.反应前后整个装置的质量不变
(4)比较两个方案,你认为哪个方案测得的碳酸钙质量分数更准确,请说明理由。
【答案】注射器活塞先是向右移动一段距离,最后又回到原位置;C
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/3 3:0:2组卷:15引用:1难度:0.5
相似题
-
 1.绍兴盛产一种四角菱,称“驮背白”。其菱肉富含淀粉等多种营养物质,此外菱角的茎和根富含纤维素(C6H10O5)n,也是一种很不错的食物和药材。
1.绍兴盛产一种四角菱,称“驮背白”。其菱肉富含淀粉等多种营养物质,此外菱角的茎和根富含纤维素(C6H10O5)n,也是一种很不错的食物和药材。
(1)菱肉中的钙、磷、铁等元素是以(填“单质”或“化合物”)的形态存在;
(2)该纤维素中C、H、O元素的质量比(最简比);
(3)查阅资料获悉菱肉制成的菱粉质细爽滑,为淀粉中之佳品。求菱叶产生3.6千克淀粉[有机物(CH2O)n]的同时,光合作用产生氧气多少千克?(已知光合作用的化学方程式为:nCO2+nH2O═(CH2O)n+nO2,条件忽略)发布:2025/1/6 8:0:1组卷:4引用:1难度:0.5 -
2.小金为测定某样品中氧化铜的质量分数,称量固体样品20.0克,用如图所示的装置进行实验(杂质不参与反应且生成水完全被吸收),实验中共消耗0.6克氢气,测得B装置反应前后的质量增加了3.6克。
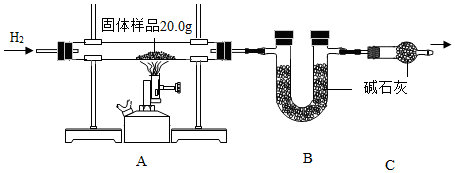
(1)C装置的作用是;
(2)计算固体样品中氧化铜的质量分数(根据化学方程式列式计算)。发布:2024/12/28 15:30:1组卷:12引用:2难度:0.5 -
3.侯德榜是我国著名的化学家,发明了侯氏制碱法,其反应原理如下:NaCl+CO2+NH3+H2O═NaHCO3+NH4Cl,请回答:
(1)反应产物中NH4C1可以用于农业生产,它属于化肥中的肥。
(2)生产16.8t碳酸氢钠,理论上需要氯化钠的质量是多少?发布:2024/12/28 15:30:1组卷:12引用:2难度:0.5


