 为寻找我国炼铜的史料,小晟同学在图书馆查阅到西汉刘安所著的《淮南万毕术》中就有“曾青得铁则化为铜”的记载,其中“曾青”指的是初中化学实验中常见试剂“CuSO4溶液”,也是农业上配制农药波尔多液所使用的药品之一。
为寻找我国炼铜的史料,小晟同学在图书馆查阅到西汉刘安所著的《淮南万毕术》中就有“曾青得铁则化为铜”的记载,其中“曾青”指的是初中化学实验中常见试剂“CuSO4溶液”,也是农业上配制农药波尔多液所使用的药品之一。
(1)农业上,配制波尔多液还需要用到一种初中常见的碱,该碱的俗称为 熟石灰或消石灰熟石灰或消石灰。
(2)“曾青得铁则化为铜”说明铁的金属活动性比铜 强强(填“强”或“弱”)。若将足量的铁粉加入一定量的ZnSO4、CuSO4混合溶液中,充分反应后溶液中所含阳离子为 Zn2+、Fe2+Zn2+、Fe2+(填离子符号)。
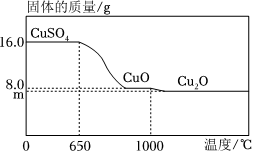
(3)为探究CuSO4的热稳定性,小晟同学将16.0gCuSO4置于坩埚中加热,在查阅相关文献资料的情况下,将测得固体质量与成分随温度变化的曲线绘制出如图所示。
【提示:SO2的沸点为-10℃,SO3的沸点为44.8℃】
①加热到650℃时,CuSO4开始发生分解反应,生成CuO和另一种氧化物X,X的化学式为 SO3SO3。
②加热到1000℃时,CuO开始分解的反应方程式为:4CuO 高温 2Cu2O+O2↑,请计算出图中m的值。(写出详细的计算过程)
(4)小晟同学通过翻阅教材,获知CuSO4溶液对H2O2的分解也具有催化作用,于是称取16gCuSO4白色粉末加入到装有192g一定量浓度的H2O2溶液的烧杯中,发现白色固体完全溶解,充分反应后烧杯中物质的总质量减轻了8g,则反应后烧杯中溶液的溶质质量分数为 8%8%。
高温
【答案】熟石灰或消石灰;强;Zn2+、Fe2+;SO3;8%
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/7/1 8:0:9组卷:91引用:3难度:0.5


