完成下列问题:
(1)已知20℃下,饱和食盐水的质量分数为26.5%,密度为1.17g/mL,则该饱和食盐水的物质的量浓度为 5.35.3mol⋅L-1。
(2)向27.2g由Fe和Fe2O3组成的固体混合物加入2L一定浓度的稀硫酸后固体恰好溶解,可收集到标准状况下气体2.24L,再向反应后的溶液中滴入KSCN溶液,无明显现象(忽略反应前后溶液的体积变化),反应后溶液中FeSO4的物质的量浓度为 0.2mol⋅L-10.2mol⋅L-1。
(3)100mL0.200mol⋅L-1CuSO4溶液与1.95g锌粉在量热计中充分反应。已知:反应Zn(s)+CuSO4(aq)═ZnSO4(aq)+Cu(s)的ΔH=-209kJ⋅mol-1,反应前后,溶液的比热容均近似为4.18J⋅g-1⋅℃-1、溶液的密度均近似为1.00g⋅cm-3,忽略溶液体积、质量变化和金属吸收的热量。实验测得反应前温度为20.1℃,请计算反应后测得的最高温度为 30.130.1℃。
【答案】5.3;0.2mol⋅L-1;30.1
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/7/27 8:0:9组卷:43引用:1难度:0.5
相似题
-
1.用25mL 18.4mol/L的浓硫酸与铜共热一段时间后,冷却,过滤除去多余的铜,将滤液稀释到100mL,所得溶液中
浓度为3mol/L,则此时溶液中CuSO4的物质的量浓度为( )SO2-4发布:2024/12/30 4:0:1组卷:138引用:6难度:0.5 -
2.标准状况下,将一充满HCl气体的烧瓶倒扣在盛有水的水槽中,HCl气体被完全吸收,假设溶液没有损失,则烧瓶内所得溶液的物质的量浓度为( )
发布:2024/12/30 6:0:2组卷:17引用:3难度:0.7 -
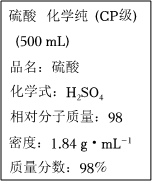 3.如图是硫酸试剂标签上的部分内容,据此下列说法正确的是( )发布:2024/12/30 4:30:1组卷:79引用:3难度:0.8
3.如图是硫酸试剂标签上的部分内容,据此下列说法正确的是( )发布:2024/12/30 4:30:1组卷:79引用:3难度:0.8


