我国著名化学家侯德榜发明的“联合制碱法”的反应原理用化学方程式可简要表示为:NH3+CO2+H2O=NH4HCO3,NH4HCO3+NaCl=NaHCO3+NH4Cl;2NaHCO3 △ Na2CO3+H2O+CO2↑。
(1)纯碱属于 盐盐(填“酸”“碱”或“盐”)。
(2)检验碳酸氢钠中含有碳酸钠的方法是 取固体少许加入适量蒸馏水溶解,然后向溶液中滴加氯化钡(或氯化钙)溶液,有白色沉淀产生,证明验碳酸氢钠固体中含有碳酸钠杂质取固体少许加入适量蒸馏水溶解,然后向溶液中滴加氯化钡(或氯化钙)溶液,有白色沉淀产生,证明验碳酸氢钠固体中含有碳酸钠杂质。
(3)NH4HCO3+NaCl=NaHCO3+NH4Cl,请写出该反应能发生的原因 由于碳酸氢钠的溶解度小,容易从溶液中析出NaHCO3晶体,导致反应的发生由于碳酸氢钠的溶解度小,容易从溶液中析出NaHCO3晶体,导致反应的发生。
(4)向含有碳酸钠和碳酸氢钠的溶液中逐滴滴加1mol/L盐酸,产生标准状况下气体的体积与盐酸体积关系如图所示:
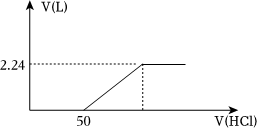
①逐滴滴加盐酸的过程中HCO-3物质的量变化趋势是 先变大,后减小先变大,后减小;
②上述混合溶液碳酸氢钠的物质的量是 0.05mol0.05mol。
△
HCO
-
3
【答案】盐;取固体少许加入适量蒸馏水溶解,然后向溶液中滴加氯化钡(或氯化钙)溶液,有白色沉淀产生,证明验碳酸氢钠固体中含有碳酸钠杂质;由于碳酸氢钠的溶解度小,容易从溶液中析出NaHCO3晶体,导致反应的发生;先变大,后减小;0.05mol
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/9/9 11:0:12组卷:171引用:2难度:0.7


