纯碱是工业生产和日常生活中的重要物质,工业纯碱中含有少量的氯化钠,某校兴趣小组的同学分别采用不同的方法测定工业纯碱样品中碳酸钠的质量分数。
【方法一】气体分析法
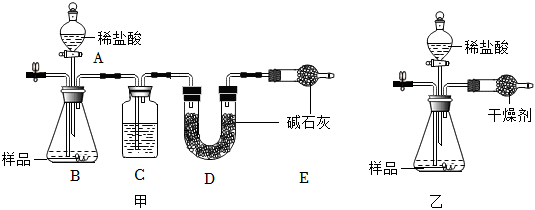
(1)甲小组同学称取一定样品,设计了如图甲所示的装置,使样品与足量的稀盐酸充分反应。通过测定反应前后D装置质量的增重量来得到CO2质量。为了避免水蒸气对实验的影响,使测得结果更准确,装置C中应装入 浓硫酸浓硫酸(填试剂名称)。
(2)乙小组同学用如图乙所示的装置实验,通过测定反应前后整个装置总质量的减轻量来得到CO2质量。根据这一思路,则所用的干燥剂应满足的条件是 吸收水蒸气、氯化氢气体,但是不能吸收二氧化碳吸收水蒸气、氯化氢气体,但是不能吸收二氧化碳。
(3)实验时,正确选择干燥剂后,为了提高测量结果的精确度,小科认为甲、乙两装置均可通过左侧导管鼓入空气一段时间,来进一步减小误差。你是否赞同他的观点,请说明理由。 不赞同,甲装置不能鼓入干燥空气,是因为干燥空气中含有二氧化碳,影响实验结果,乙装置反应前后鼓入干燥空气,能使生成的二氧化碳全部逸出,实验结果更准确不赞同,甲装置不能鼓入干燥空气,是因为干燥空气中含有二氧化碳,影响实验结果,乙装置反应前后鼓入干燥空气,能使生成的二氧化碳全部逸出,实验结果更准确。
【方法二】沉淀分析法
(4)兴趣小组为测定该工业纯碱中Na2CO3的质量分数,称取40g该样品,平均分为四份,加水充分溶解,然后分别加入一定质量分数的CaCl2溶液,实验数据见下表:
| 实验一 | 实验二 | 实验三 | 实验四 | |
| 工业纯碱样品质量 | 10g | 10g | 10g | 10g |
| 加入CaCl2溶液的质量 | 20g | 40g | 60g | 80g |
| 反应生成沉淀的质量 | 2g | 4g | 5g | 5g |
【考点】根据化学反应方程式的计算;化学实验方案的设计与评价.
【答案】浓硫酸;吸收水蒸气、氯化氢气体,但是不能吸收二氧化碳;不赞同,甲装置不能鼓入干燥空气,是因为干燥空气中含有二氧化碳,影响实验结果,乙装置反应前后鼓入干燥空气,能使生成的二氧化碳全部逸出,实验结果更准确
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/8/30 0:0:8组卷:11引用:1难度:0.5
相似题
-
 1.绍兴盛产一种四角菱,称“驮背白”。其菱肉富含淀粉等多种营养物质,此外菱角的茎和根富含纤维素(C6H10O5)n,也是一种很不错的食物和药材。
1.绍兴盛产一种四角菱,称“驮背白”。其菱肉富含淀粉等多种营养物质,此外菱角的茎和根富含纤维素(C6H10O5)n,也是一种很不错的食物和药材。
(1)菱肉中的钙、磷、铁等元素是以(填“单质”或“化合物”)的形态存在;
(2)该纤维素中C、H、O元素的质量比(最简比);
(3)查阅资料获悉菱肉制成的菱粉质细爽滑,为淀粉中之佳品。求菱叶产生3.6千克淀粉[有机物(CH2O)n]的同时,光合作用产生氧气多少千克?(已知光合作用的化学方程式为:nCO2+nH2O═(CH2O)n+nO2,条件忽略)发布:2025/1/6 8:0:1组卷:4引用:1难度:0.5 -
2.小金为测定某样品中氧化铜的质量分数,称量固体样品20.0克,用如图所示的装置进行实验(杂质不参与反应且生成水完全被吸收),实验中共消耗0.6克氢气,测得B装置反应前后的质量增加了3.6克。
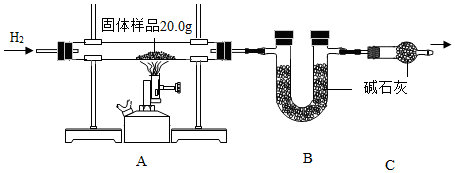
(1)C装置的作用是;
(2)计算固体样品中氧化铜的质量分数(根据化学方程式列式计算)。发布:2024/12/28 15:30:1组卷:12引用:2难度:0.5 -
3.侯德榜是我国著名的化学家,发明了侯氏制碱法,其反应原理如下:NaCl+CO2+NH3+H2O═NaHCO3+NH4Cl,请回答:
(1)反应产物中NH4C1可以用于农业生产,它属于化肥中的肥。
(2)生产16.8t碳酸氢钠,理论上需要氯化钠的质量是多少?发布:2024/12/28 15:30:1组卷:12引用:2难度:0.5


