某化学兴趣小组为探究Cl2的性质并制备氯水,用如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
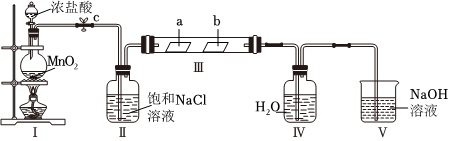
回答下列问题:
(1)盛装浓盐酸的仪器的名称为 分液漏斗分液漏斗。
(2)装置Ⅰ中发生反应的化学方程式为 MnO2+4HCl △ MnCl2+Cl2↑+2H2OMnO2+4HCl △ MnCl2+Cl2↑+2H2O。
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为应在 ⅡⅡ和 ⅢⅢ(填装置序号)之间添加洗气装置,该装置的作用是 干燥Cl2干燥Cl2。
(4)装置Ⅴ中NaOH溶液的作用是 吸收多余的Cl2,防止污染环境吸收多余的Cl2,防止污染环境,相关反应的离子方程式为 Cl2+2OH-=ClO-+Cl-+H2OCl2+2OH-=ClO-+Cl-+H2O。
(5)工业上可用氢氧化钠与氯气反应制取84消毒液,在生活中84消毒液不可与洁厕灵(HCl)混用,否则会产生一种黄绿有毒气体,其原因是 2H++ClO-+Cl-=Cl2↑+H2O2H++ClO-+Cl-=Cl2↑+H2O(用离子方程式解释)
(6)氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强,氯水中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图1所示。
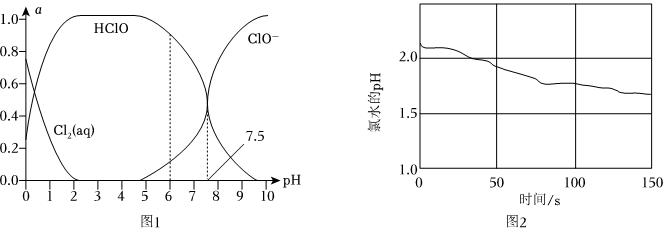
①用氯处理饮用水,pH=7.5时的杀菌效果比pH=6.5时的杀菌效果 差差(填“好”或“差”)。
②利用数字化实验测定光照氯水得到光照过程中氯水的pH变化情况如图2所示,变化原因是 次氯酸见光分解生成盐酸,酸性增强(或2HClO 光 2HCl+O2↑)次氯酸见光分解生成盐酸,酸性增强(或2HClO 光 2HCl+O2↑)(用方程式或必要的文字说明)
△
△
光
光
【答案】分液漏斗;MnO2+4HCl MnCl2+Cl2↑+2H2O;Ⅱ;Ⅲ;干燥Cl2;吸收多余的Cl2,防止污染环境;Cl2+2OH-=ClO-+Cl-+H2O;2H++ClO-+Cl-=Cl2↑+H2O;差;次氯酸见光分解生成盐酸,酸性增强(或2HClO 2HCl+O2↑)
△
光
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/17 15:0:1组卷:54引用:1难度:0.7
相似题
-
1.为了验证干燥的氯气无漂白性,湿润的氯气具有漂白性,某同学设计实验如图.其中B、C、D、E、F分别盛有饱和食盐水、浓硫酸.干燥红色布条、浓硫酸、湿润红色布条.
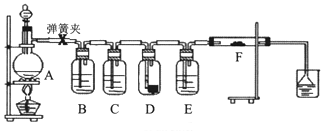
请回答:
(1)E中浓硫酸的作用.
(2)将F中的湿润布条换成卷曲的细铜丝,并用酒精灯加热,可看到的现象是.
(3)若用装置A制取2.24L(标况)氯气,消耗10mol/L浓盐酸的体积明显大于40mL,造成该结果的可能原因有.
A.浓盐酸的挥发 B.随反应进行盐酸浓度下降
C.加热时火力不够猛 D.MnO2固体过量.发布:2025/1/15 8:0:2组卷:17引用:1难度:0.3 -
2.如图是某同学设计的氯气制备及性质验证实验装置。相关说法正确的是( )
 发布:2025/1/15 8:0:2组卷:21引用:2难度:0.8
发布:2025/1/15 8:0:2组卷:21引用:2难度:0.8 -
3.实验室中模拟用甲烷与氯气反应得到的副产品来制取盐酸,原理如图,下列说法不正确的是( )
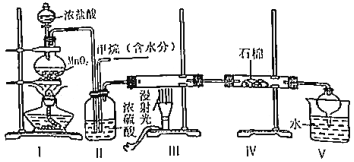 发布:2024/12/30 17:0:5组卷:61引用:1难度:0.7
发布:2024/12/30 17:0:5组卷:61引用:1难度:0.7


