已知过氧化钠(Na2O2)为淡黄色粉末,可溶于水,可分别与水、二氧化碳反应。过氧化钠与水反应生成氢氧化钠和氧气,与二氧化碳反应生成碳酸钠和氧气。现有一瓶放置较长时间的过氧化钠粉末,已部分变质,小明同学为探究其成分,取17.1g该粉末再加入100g水充分反应,测得最后剩余物的质量为115.5g。
(1)过氧化钠与水反应生成氧气的质量为1.61.6g;
(2)在加入100 g水后的溶液中再加入稀盐酸,共收集到2.2 g CO2,则固体粉末中碳酸钠的质量分数为多少?(写出计算过程,计算结果精确到0.1%)
(3)在加入100 g水后的溶液中再加入稀盐酸,所加盐酸质量与生成气体的总质量关系如表格:
| 次数 | 1次 | 2次 | 3次 | 4次 | 5次 |
| 加入稀盐酸的质量/g | 25 | 25 | 25 | 25 | 25 |
| 生成气体的总质量/g | 0 | a | 0 | 2.2 | b |
2.2
2.2
g【考点】根据化学反应方程式的计算;质量守恒定律及其应用.
【答案】1.6;2.2
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/9/21 0:0:8组卷:46引用:1难度:0.5
相似题
-
1.小金为测定某样品中氧化铜的质量分数,称量固体样品20.0克,用如图所示的装置进行实验(杂质不参与反应且生成水完全被吸收),实验中共消耗0.6克氢气,测得B装置反应前后的质量增加了3.6克。
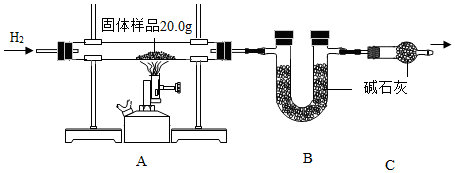
(1)C装置的作用是;
(2)计算固体样品中氧化铜的质量分数(根据化学方程式列式计算)。发布:2024/12/28 15:30:1组卷:12引用:2难度:0.5 -
 2.绍兴盛产一种四角菱,称“驮背白”。其菱肉富含淀粉等多种营养物质,此外菱角的茎和根富含纤维素(C6H10O5)n,也是一种很不错的食物和药材。
2.绍兴盛产一种四角菱,称“驮背白”。其菱肉富含淀粉等多种营养物质,此外菱角的茎和根富含纤维素(C6H10O5)n,也是一种很不错的食物和药材。
(1)菱肉中的钙、磷、铁等元素是以(填“单质”或“化合物”)的形态存在;
(2)该纤维素中C、H、O元素的质量比(最简比);
(3)查阅资料获悉菱肉制成的菱粉质细爽滑,为淀粉中之佳品。求菱叶产生3.6千克淀粉[有机物(CH2O)n]的同时,光合作用产生氧气多少千克?(已知光合作用的化学方程式为:nCO2+nH2O═(CH2O)n+nO2,条件忽略)发布:2025/1/6 8:0:1组卷:4引用:1难度:0.5 -
3.侯德榜是我国著名的化学家,发明了侯氏制碱法,其反应原理如下:NaCl+CO2+NH3+H2O═NaHCO3+NH4Cl,请回答:
(1)反应产物中NH4C1可以用于农业生产,它属于化肥中的肥。
(2)生产16.8t碳酸氢钠,理论上需要氯化钠的质量是多少?发布:2024/12/28 15:30:1组卷:12引用:2难度:0.5


