无水三氯化铁呈棕红色,易潮解,100℃左右时升华,冷却后易凝华。如图是两名学生设计的用氯气与铁反应制备无水三氯化铁的实验装置。左边的反应装置相同,而右边的产品收集装置则不同,分别如(Ⅰ)和(Ⅱ)所示。试回答:
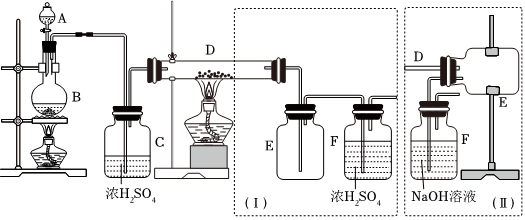
(1)A仪器的名称是 分液漏斗分液漏斗;
(2)B中反应的离子方程式为 MnO2+4H++2Cl- △ Mn2++Cl2↑+2H2OMnO2+4H++2Cl- △ Mn2++Cl2↑+2H2O;其中浓盐酸表现出 酸、还原酸、还原性;若用含有0.2mol HCl的浓盐酸与足量的MnO2反应制取Cl2,制得的Cl2体积总是小于1.12L(标准状况)的原因是 随着反应的进行,浓盐酸的浓度逐渐减小变为稀盐酸,反应停止随着反应的进行,浓盐酸的浓度逐渐减小变为稀盐酸,反应停止。
(3)气体通过装置C的目的是 吸收水蒸气,干燥氯气吸收水蒸气,干燥氯气。
(4)D中的反应开始前,需进行的操作是 排除装置中的空气排除装置中的空气,应采取的方法是 B中的反应进行一段时间后,看到黄绿色气体充满整个装置,再开始加热DB中的反应进行一段时间后,看到黄绿色气体充满整个装置,再开始加热D。
(5)D中发生反应的化学方程式为 2Fe+3Cl2 △ 2FeCl32Fe+3Cl2 △ 2FeCl3。
(6)装置(Ⅰ)的主要缺点是 氯化铁升华后遇冷凝华,导管易被堵塞;尾气排入空气,会造成环境污染氯化铁升华后遇冷凝华,导管易被堵塞;尾气排入空气,会造成环境污染。
(7)装置(Ⅱ)中F中发生反应的化学方程式为 2NaOH+Cl2═NaCl+NaClO+H2O2NaOH+Cl2═NaCl+NaClO+H2O。如果选用(Ⅱ)装置来完成实验,则必须采取的改进措施是 在瓶E和F之间连接装有干燥剂的装置(其他既能防止产品潮解又能防止尾气污染环境的合理答案均给分)在瓶E和F之间连接装有干燥剂的装置(其他既能防止产品潮解又能防止尾气污染环境的合理答案均给分)。
△
△
△
△
【答案】分液漏斗;MnO2+4H++2Cl- Mn2++Cl2↑+2H2O;酸、还原;随着反应的进行,浓盐酸的浓度逐渐减小变为稀盐酸,反应停止;吸收水蒸气,干燥氯气;排除装置中的空气;B中的反应进行一段时间后,看到黄绿色气体充满整个装置,再开始加热D;2Fe+3Cl2 2FeCl3;氯化铁升华后遇冷凝华,导管易被堵塞;尾气排入空气,会造成环境污染;2NaOH+Cl2═NaCl+NaClO+H2O;在瓶E和F之间连接装有干燥剂的装置(其他既能防止产品潮解又能防止尾气污染环境的合理答案均给分)
△
△
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/7/18 8:0:9组卷:102引用:2难度:0.4
相似题
-
1.硫铁矿烧渣是硫铁矿生产硫酸过程中产生的工业废渣(主要含Fe2O3及少量SiO2、Al2O3等杂质).用该烧渣制取药用辅料--红氧化铁的工艺流程如下:
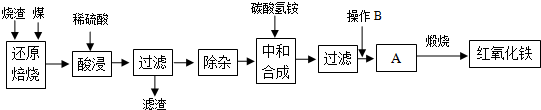
(1)在“还原焙烧”中产生的有毒气体可能有.
(2)“酸浸”时间一般不超过20min,若在空气中酸浸时间过长,溶液中Fe2+含量将下降,其原因是(用离子方程式表示).
(3)根据下表数据:
在“除杂”步骤中,为除去Fe3+和Al3+,溶液的pH最大值应小于氢氧化物 Al(OH)3 Fe(OH)3 Fe(OH)2 开始沉淀的pH 3.10 2.01 7.11 完全沉淀的pH 4.77 3.68 9.61 ,检验
Fe3+已经除尽的试剂是.
(4)“中和合成”的目的是将溶液中Fe2+转变为碳酸亚铁沉淀,则操作B是.
(5)煅烧A的反应方程式是.
(6)a g烧渣经过上述工艺可得红氧化铁b g.药典标准规定,制得的红氧化铁中含氧化铁不得少于98.0%,则所选用的烧渣中铁的质量分数应不低于(用含a、b的表达式表示).发布:2025/1/19 8:0:1组卷:5引用:1难度:0.5 -
2.硫铁矿烧渣是硫铁矿生产硫酸过程中产生的工业废渣(主要含Fe2O3及少量SiO2、Al2O3、CaO、MgO等杂质).用该烧渣制取药用辅料--红氧化铁的工艺流程如图:
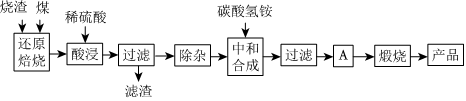
(1)在“还原焙烧”中产生的有毒气体可能有.
(2)“酸浸”时间一般不超过20min,若在空气中酸浸时间过长,溶液中Fe2+含量将下降,其原因是(用离子方程式表示).
(3)根据下表数据:
在“除杂”步骤中,为除去Fe3+和Al3+,溶液的pH最大值应小于氢氧化物 Al(OH)3 Mg(OH)2 Fe(OH)3 Fe(OH)2 开始沉淀的pH 3.10 8.54 2.01 7.11 完全沉淀的pH 4.77 11.04 3.68 9.61 ,检验Fe3+已经除尽的试剂是;当pH=5时,溶液中c(Al3+)=mol•L-1(已知常温下Ksp[Al(OH)3]=2.0×10-33).
(4)“中和合成”的目的是将溶液中Fe2+转变为碳酸亚铁沉淀,则A的操作是.
(5)a g烧渣经过上述工艺可得红氧化铁b g.药典标准规定,制得的红氧化铁中含氧化铁不得少于98.0%,则所选用的烧渣中铁的质量分数应不低于(用含a、b的表达式表示).发布:2025/1/19 8:0:1组卷:114引用:4难度:0.5 -
3.硫铁矿烧渣是硫铁矿生产硫酸过程中产生的工业废渣(主要含Fe2O3及少量SiO2、Al2O3、CaO、MgO等杂质).用该烧渣制取药用辅料--红氧化铁的工艺流程如下:
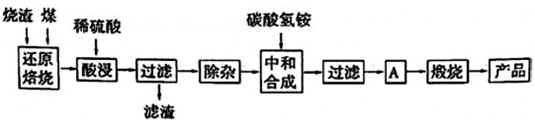
(1)在“还原焙烧”中产生的有毒气体可能有.
(2)“酸浸”时间一般不超过20min,若在空气中酸浸时间过长,溶液中Fe2+含量将下降,其原因是(用离子方程式表示).
(3)根据下表数据:
在“除杂”步骤中,为除去Fe3+和Al3+,溶液的pH最大值应小于氢氧化物 Al(OH)3 Mg(OH)2 Fe(OH)3 Fe(OH)2 开始沉淀的pH 3.10 8.54 2.01 7.11 完全沉淀的pH 4.77 11.04 3.68 9.61 ,常温下,当pH=5时,溶液中c(Al3+)=mol•L-1(已知常温下Ksp[Al(OH)3]═2.0×10-33).
(4)“中和合成”的目的是将溶液中Fe2+转变为碳酸亚铁沉淀,则A的操作是.发布:2025/1/19 8:0:1组卷:12引用:1难度:0.5


