K3[Fe(C2O4)3]⋅3H2O(三草酸合铁酸钾)是制备负载型活性铁催化剂的主要原料.回答下列问题:
Ⅰ.现利用如图装置检验三草酸合铁酸钾受热分解所得产物中是否含有CO,CO2。
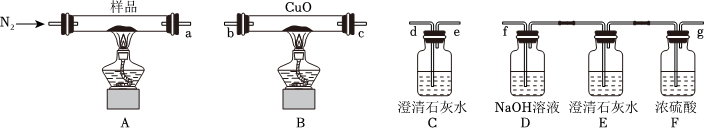
(1)正确的连接顺序为a→f→g→b→c→d或f→g→c→b→df→g→b→c→d或f→g→c→b→d(填小写标号,仪器可重复使用)。
(2)实验过程中需持续通入N2的目的是 将生成的CO、CO2转移到后续的检验装置中将生成的CO、CO2转移到后续的检验装置中、防止二氧化碳与氢氧化钠溶液反应导致溶液倒吸防止二氧化碳与氢氧化钠溶液反应导致溶液倒吸。
(3)证明产物中有CO的现象是 E中澄清石灰水不变浑浊,B中硬质玻璃管中黑色固体变红且C中澄清石灰水变浑浊E中澄清石灰水不变浑浊,B中硬质玻璃管中黑色固体变红且C中澄清石灰水变浑浊。
(4)样品完全分解后,装置A中残留物含有FeO和Fe2O3,请利用所给试剂设计实验方案证明存在FeO 残留物溶解到稀硫酸溶液中,待其完全溶解后滴加几滴高锰酸钾溶液,若高锰酸钾溶液的紫色褪去,则混合物中存在FeO残留物溶解到稀硫酸溶液中,待其完全溶解后滴加几滴高锰酸钾溶液,若高锰酸钾溶液的紫色褪去,则混合物中存在FeO(要求写出操作、现象和结论)。
提供试剂:稀盐酸、稀硫酸、KSCN溶液、氯水、NaOH溶液、KMnO4溶液
Ⅱ.测定三草酸合铁酸钾中铁元素的含量。
(1)称取mg三草酸合铁酸钾样品(摩尔质量为Mg⋅mol-1),溶于水配成250mL溶液,所需玻璃仪器除烧杯、玻璃棒、量筒外还有 250mL容量瓶250mL容量瓶(填仪器名称)。
(2)取25mL上述溶液于锥形瓶中,加入稀硫酸酸化,再滴加KMnO4溶液至与C2O2-4恰好反应,反应的离子方程式为 5H2C2O2-4+2MnO-4+6H+=10CO2↑+2Mn2++8H2O5H2C2O2-4+2MnO-4+6H+=10CO2↑+2Mn2++8H2O。
(3)向(2)反应后溶液中加入适量还原剂将Fe3+恰好完全还原为Fe2+,加入稀硫酸酸化后,继续加cmol⋅L-1VmLKMnO4溶液时恰好与Fe2+反应.晶体中铁元素的质量分数表达式为 5 cv×561000m×100%5 cv×561000m×100%%,若配制样品溶液定容时俯视读数会导致测定结果 偏高偏高(填偏高、偏低或无影响)。
O
2
-
4
O
2
-
4
M
n
O
-
4
O
2
-
4
M
n
O
-
4
5
cv
×
56
1000
m
5
cv
×
56
1000
m
【考点】制备实验方案的设计;探究物质的组成或测量物质的含量.
【答案】f→g→b→c→d或f→g→c→b→d;将生成的CO、CO2转移到后续的检验装置中;防止二氧化碳与氢氧化钠溶液反应导致溶液倒吸;E中澄清石灰水不变浑浊,B中硬质玻璃管中黑色固体变红且C中澄清石灰水变浑浊;残留物溶解到稀硫酸溶液中,待其完全溶解后滴加几滴高锰酸钾溶液,若高锰酸钾溶液的紫色褪去,则混合物中存在FeO;250mL容量瓶;5H2C2+2+6H+=10CO2↑+2Mn2++8H2O; ×100%;偏高
O
2
-
4
M
n
O
-
4
5
cv
×
56
1000
m
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/7/12 8:0:9组卷:22引用:1难度:0.5
相似题
-
1.硫铁矿烧渣是硫铁矿生产硫酸过程中产生的工业废渣(主要含Fe2O3及少量SiO2、Al2O3、CaO、MgO等杂质).用该烧渣制取药用辅料--红氧化铁的工艺流程如图:
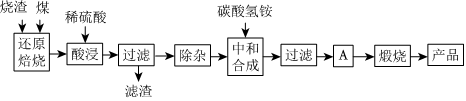
(1)在“还原焙烧”中产生的有毒气体可能有.
(2)“酸浸”时间一般不超过20min,若在空气中酸浸时间过长,溶液中Fe2+含量将下降,其原因是(用离子方程式表示).
(3)根据下表数据:
在“除杂”步骤中,为除去Fe3+和Al3+,溶液的pH最大值应小于氢氧化物 Al(OH)3 Mg(OH)2 Fe(OH)3 Fe(OH)2 开始沉淀的pH 3.10 8.54 2.01 7.11 完全沉淀的pH 4.77 11.04 3.68 9.61 ,检验Fe3+已经除尽的试剂是;当pH=5时,溶液中c(Al3+)=mol•L-1(已知常温下Ksp[Al(OH)3]=2.0×10-33).
(4)“中和合成”的目的是将溶液中Fe2+转变为碳酸亚铁沉淀,则A的操作是.
(5)a g烧渣经过上述工艺可得红氧化铁b g.药典标准规定,制得的红氧化铁中含氧化铁不得少于98.0%,则所选用的烧渣中铁的质量分数应不低于(用含a、b的表达式表示).发布:2025/1/19 8:0:1组卷:114引用:4难度:0.5 -
2.硫铁矿烧渣是硫铁矿生产硫酸过程中产生的工业废渣(主要含Fe2O3及少量SiO2、Al2O3等杂质).用该烧渣制取药用辅料--红氧化铁的工艺流程如下:
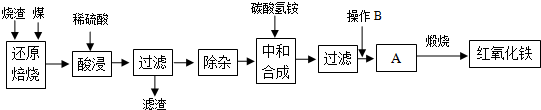
(1)在“还原焙烧”中产生的有毒气体可能有.
(2)“酸浸”时间一般不超过20min,若在空气中酸浸时间过长,溶液中Fe2+含量将下降,其原因是(用离子方程式表示).
(3)根据下表数据:
在“除杂”步骤中,为除去Fe3+和Al3+,溶液的pH最大值应小于氢氧化物 Al(OH)3 Fe(OH)3 Fe(OH)2 开始沉淀的pH 3.10 2.01 7.11 完全沉淀的pH 4.77 3.68 9.61 ,检验
Fe3+已经除尽的试剂是.
(4)“中和合成”的目的是将溶液中Fe2+转变为碳酸亚铁沉淀,则操作B是.
(5)煅烧A的反应方程式是.
(6)a g烧渣经过上述工艺可得红氧化铁b g.药典标准规定,制得的红氧化铁中含氧化铁不得少于98.0%,则所选用的烧渣中铁的质量分数应不低于(用含a、b的表达式表示).发布:2025/1/19 8:0:1组卷:5引用:1难度:0.5 -
3.硫铁矿烧渣是硫铁矿生产硫酸过程中产生的工业废渣(主要含Fe2O3及少量SiO2、Al2O3、CaO、MgO等杂质).用该烧渣制取药用辅料--红氧化铁的工艺流程如下:
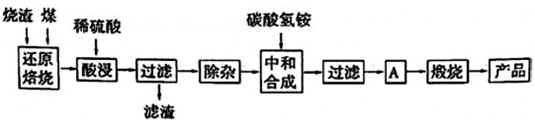
(1)在“还原焙烧”中产生的有毒气体可能有.
(2)“酸浸”时间一般不超过20min,若在空气中酸浸时间过长,溶液中Fe2+含量将下降,其原因是(用离子方程式表示).
(3)根据下表数据:
在“除杂”步骤中,为除去Fe3+和Al3+,溶液的pH最大值应小于氢氧化物 Al(OH)3 Mg(OH)2 Fe(OH)3 Fe(OH)2 开始沉淀的pH 3.10 8.54 2.01 7.11 完全沉淀的pH 4.77 11.04 3.68 9.61 ,常温下,当pH=5时,溶液中c(Al3+)=mol•L-1(已知常温下Ksp[Al(OH)3]═2.0×10-33).
(4)“中和合成”的目的是将溶液中Fe2+转变为碳酸亚铁沉淀,则A的操作是.发布:2025/1/19 8:0:1组卷:12引用:1难度:0.5


