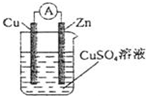
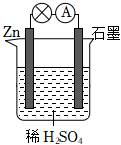
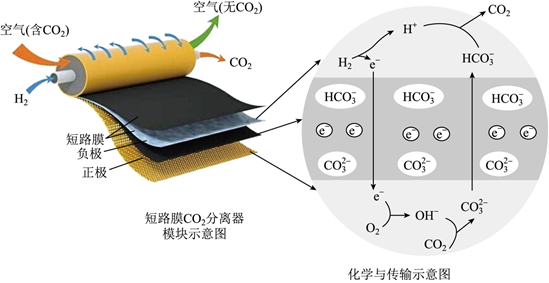
根据所学电化学知识,回答下列问题: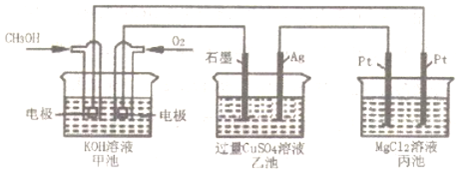
(1)①甲池中通入CH3OH的电极名称是负负极,写出其电极反应式CH3OH-6e-+8OH-=CO32-+6H2OCH3OH-6e-+8OH-=CO32-+6H2O;乙池中石墨电极反应式为4 OH--4e-=O2↑+2H2O4 OH--4e-=O2↑+2H2O;丙池中反应的离子方程式为Mg2++2Cl-+2H2O 电解 Mg(OH)2↓+H2↑+Cl2↑Mg2++2Cl-+2H2O 电解 Mg(OH)2↓+H2↑+Cl2↑;
②反应一段时间后,甲池中消耗560mL (标准状况下) O2,此时乙池溶液的pH=00;若向乙池中加入CuOCuO,其质量为44g,能使CuSO4溶液恢复到原浓度(假设电解前后溶液的体积不变,均为100mL)。丙池中理论上最多产生2.92.9g 固体。
(2)工业上以石墨为电极,电解CuCl2溶液时,发现阴极上也会有CuCl析出,写出此过程中阴极上的电极反应式Cu2++e-+Cl-=CuClCu2++e-+Cl-=CuCl。
电解
电解
【考点】原电池与电解池的综合.
【答案】负;CH3OH-6e-+8OH-=CO32-+6H2O;4 OH--4e-=O2↑+2H2O;Mg2++2Cl-+2H2O Mg(OH)2↓+H2↑+Cl2↑;0;CuO;4;2.9;Cu2++e-+Cl-=CuCl
电解
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/8/16 12:0:1组卷:73引用:2难度:0.4