碳热还原法是一种在一定温度下以无机碳为还原剂进行氧化还原反应的方法,在冶金行业有着广泛的应用。
回答下列问题:
(1)氧化铝碳热还原过程发生了如下反应:
2Al2O3(s)+9C(s)=Al4C3(s)+6CO(g)ΔH1 反应初始温度1714K
2Al2O3(s)+3C(s)=Al4O4C(s)+2CO(g)ΔH2 反应初始温度1689K
Al4O4C(s)+6C(s)=Al4C3(s)+4CO(g)ΔH3 反应初始温度1726K
①ΔH3=ΔH1-ΔH2ΔH1-ΔH2(用含ΔH1、ΔH2的代数式表示)。
②根据以上信息分析,在相同系统压力下,1700K时,Al2O3与C反应优先生成的含铝化合物为 Al4O4CAl4O4C(填化学式)。
(2)科学家在氧化铝碳热还原法研究中加入无水氯化铝作氯化剂,一定条件下,氧化铝先转化为Al4O4C和Al4C3,Al4O4C和Al4C3再转化为低价氯化铝(AlCl),低价氯化铝进入低温区歧化得到铝。忽略中间产物,写出由氧化铝直接获得AlCl的化学方程式:Al2O3+AlCl3+3C 一定条件 3AlCl+3COAl2O3+AlCl3+3C 一定条件 3AlCl+3CO。
(3)三氯化铝固体在一定温度与压强下升华,可能生成三氯化铝气体[AlCl3(s)→AlCl3(g)反应i],也可能生成六氯化二铝气体[2AlCl3(s)→Al2Cl6(g)反应ii],实验结果如图所示:

①在10~100Pa,350~370K条件下,氯化铝升华得到 AlCl3AlCl3(填AlCl3或Al2Cl6)。
②气态氯化铝是具有配位键的化合物,分子中原子间成键关系如图所示,请将图中你认为是配位键的斜线上加上箭头 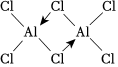
 。
。

(4)碳热还原制锰合金反应为Mn3C(s)+CO2(g)⇌3Mn(s)+2CO(g)Kp,CO与CO2平衡分压比的自然对数值(1nK=2.303×lgK)与温度的关系如图所示(已知KP是用平衡分压代替浓度计算所得的平衡常数,分压=总压×气体的物质的量分数)。

向恒容密闭容器中加入足量Mn3C并充入0.1molCO2,发生上述反应,测得A点时容器的总压为akPa,则A点时CO2的平衡转化率为 33.3%33.3%(保留三位有效数字);A点对应温度下的Kp=0.5a0.5akPa。
一定条件
一定条件


【答案】ΔH1-ΔH2;Al4O4C;Al2O3+AlCl3+3C 3AlCl+3CO;AlCl3; ;33.3%;0.5a
;33.3%;0.5a
一定条件
 ;33.3%;0.5a
;33.3%;0.5a【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/5/12 8:0:9组卷:51引用:3难度:0.7
相似题
-
1.氢气最早于16世纪被人工制取出来,氢气是一种清洁能源。
(1)利用光伏电池电解水制H2是氢能的重要来源。已知:H-H键、O=O键、H-O键的键能依次为436kJ•mol-1、495kJ•mol-1、463kJ•mol-1。则2H2O(g)═2H2(g)+O2(g)△H=kJ•mol-1。
(2)T1℃时,向5L恒容密闭容器中充入0.5molCH4,只发生反应2CH4(g)⇌C2H4(g)+2H2(g),达到平衡时,测得c(C2H4)=2c(CH4),CH4的转化率为;保持其他条件不变,温度改为T2℃,经25s后达到平衡,测得c(CH4)=2c(C2H4),则0~25s内v(C2H4)=mol•L-1•s-1。
(3)CH4分解时几种气体的平衡分压(pPa)的对数值lgp与温度的关系如图所示。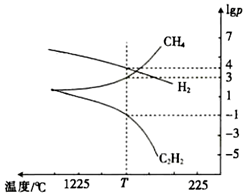
①T℃时,向一恒容密闭容器中通入一定量的CH4(g)、C2H4(g)和H2(g),只发生反应2CH4(g)⇌C2H2(g)+3H2(g)ΔH,ΔH(填“>”或“<”)0,此时的平衡常数Kp=(用平衡分压代替浓度进行计算)Pa2。
②若只改变一个反应条件使Kp变大,则该条件是(填标号)。
A.减小C2H2的浓度
B.升高温度
C.增大压强
D.加入合适的催化剂
(4)工业上,以KNH2和液氨为电解质,以石墨为电极,电解液氨制备H2。阳极的电极反应式为,一段时间后阴、阳两极收集到的气体质量之比为。发布:2025/1/4 8:0:1组卷:9引用:3难度:0.5 -
2.反应 4A(g)+5B(g)⇌4C(g)+6D(g)在 5L 的密闭容器中进行,半分钟后,C 的物质的量增 加了 0.30mol。下列叙述正确的是( )
发布:2024/12/30 19:30:2组卷:67引用:6难度:0.6 -
3.将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)⇌xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,c(A):c(B)=3:5,C的平均反应速率为0.1mol/(L•min).求:
(1)此时A的浓度c(A)=mol/L,反应开始前容器中的A、B的物质的量:n(A)=n(B)=mol;
(2)B的平均反应速率v(B)=mol/(L•min);
(3)x的值为.发布:2024/12/30 19:0:1组卷:164引用:26难度:0.3
相关试卷


