氧气是一种重要的气体,人们一直寻找通过各种方法获得所需的氧气。
(一)实验室制氧气
在相同的条件下,某同学用加热氯酸钾的方法制取氧气,并对催化剂进行探究:
| 编号 | KClO3质量/g | 催化剂 | 催化剂质量/g | 收集50mLO2所需时间/s |
| 实验1 | 5 | 171 | ||
| 实验2 | 5 | MnO2 | 0.5 | 49 |
| 实验3 | 5 | Fe2O3 | 0.5 | 58 |
| 实验4 | 5 | KCl | 0.5 | 154 |
2KClO3 2KCl+3O2↑
M
n
O
2
△
2KClO3 2KCl+3O2↑
。M
n
O
2
△
(2)表中所列3种催化剂的催化效果最佳的是
MnO2
MnO2
。(3)由实验4和实验
1
1
可知,KCl有催化作用。维持加热条件不变,用实验1再继续收集收集50mLO2,所需时间明显少于171s,解释原因 生成的氯化钾加快了反应速率
生成的氯化钾加快了反应速率
。(4)要比较KClO3分解反应中不同催化剂的催化效果,除了可以通过测量收集50mLO2所需时间的方法外,还可以通过测量
相同时间收集气体体积的大小
相同时间收集气体体积的大小
的方法可知。(二)家庭中制氧气
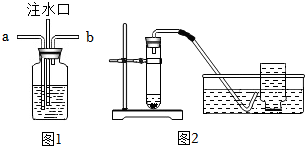
(1)某家庭制氧机上有湿化瓶装置。人吸氧时观察到瓶中有气泡。湿化瓶装置类似于图1。关于该装置,下列说法正确的有
BCD
BCD
(填字母序号)。A.b导管连接制氧机
B.b导管连接人吸氧气的塑料管
C.使用该装置可以观测是否有氧气输出
D.使用该装置可以观测氧气输出的速率
(三)渔业制氧气
(1)运输活鱼时,用过氧化钙(CaO2)可增加水中含氧量。联想到过氧化钙(CaO2)的此作用,某同学在实验时,提出下列猜想并用图2装置进行实验:
【猜想】CaO2与H2O反应用于实验室制取氧气。
【实验过程】
①组装仪器,
检查装置气密性
检查装置气密性
(填一实验步骤)。②向试管中加入CaO2和H2O后,有极微量细小气泡缓慢放出。将导管伸入集气瓶中,几乎收集不到气体。放置到第二天,集气瓶中只收集到少量气体,振荡试管后仍有极微量细小气泡缓慢放出。
【实验结论】CaO2与H2O反应
不能
不能
(填“能”或“不能”)用于实验室制取氧气。(2)以下是一种制备过氧化钙晶体(CaO2•8H2O)的实验方法。回答下列问题:
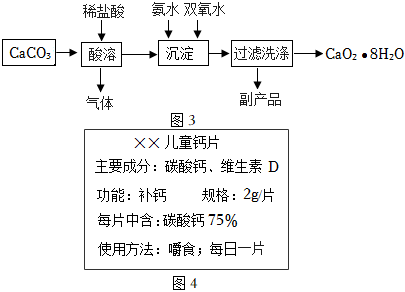
【资料】双氧水不稳定,受热易分解。(图3)
①沉淀池中的化学反应需要在冰水中进行,原因有
双氧水受热易分解
双氧水受热易分解
(任答一点)。②碳酸钙可以作为补钙剂,钙元素
不是
不是
(填“是”或“不是”)人体所需的微量元素,儿童缺钙易患 佝偻
佝偻
病。如图4为某钙片的商品标签,按标签计算,则每片能补充钙元素 0.6
0.6
g。③已知CaO2•8H2O 的相对分子质量为216,现测得该所制得的过氧化钙晶体中,CaO2•8H2O 的质量分数为86.4%(产品中其它成分不含钙元素),则该晶体中钙元素的质量分数为
16%
16%
(写出解题过程)。【考点】影响化学反应速率的因素探究;催化剂的特点与催化作用.
【答案】2KClO3 2KCl+3O2↑;MnO2;1;生成的氯化钾加快了反应速率;相同时间收集气体体积的大小;BCD;检查装置气密性;不能;双氧水受热易分解;不是;佝偻;0.6;16%
M
n
O
2
△
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/9/12 4:0:8组卷:42引用:1难度:0.5
相似题
-
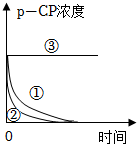 1.Fenton法常用于处理含难降解有机物的工业废水。其原理是利用Fe2+和H2O2的反应产生能降解污染物的活性成分。现运用该方法降解有机污染物p-CP,探究有关因素对降解反应速率的影响。实验探究:控制p-CP的初始浓度相同,实验温度恒定在25℃或40℃(其余实验条件见下表)。
1.Fenton法常用于处理含难降解有机物的工业废水。其原理是利用Fe2+和H2O2的反应产生能降解污染物的活性成分。现运用该方法降解有机污染物p-CP,探究有关因素对降解反应速率的影响。实验探究:控制p-CP的初始浓度相同,实验温度恒定在25℃或40℃(其余实验条件见下表)。
(1)请结合上述介绍将表中空格补充完整。
(2)实验测得p-CP的浓度随时间变化的关系如图所示,根据实验①、②图像可得出结论:实验编号 实验目的 温度/℃
pH浓度/(mg•L﹣1) H2O2 Fe2+ ① 为②③提供参照 25 3 204 16.8 ② 探究温度对降解反应速率的影响
3 204 16.8 ③ 探究溶液pH对降解反应速率的影响 25 10 204 16.8 。
(3)为测定不同时间内有机物降解的浓度,需在不同时间从反应器中取样,并使所取样品中的降解反应立即停止下来。根据本题信息,将样品从反应器中取出后应立即将其放入某药品中,反应会迅速停止,该药品可能是。
A盐酸溶液 B氢氧化钠溶液 C稀硫酸溶液 D碳酸钠溶液发布:2024/11/25 8:0:2组卷:3引用:0难度:0.3 -
2.据图1装置图回答问题
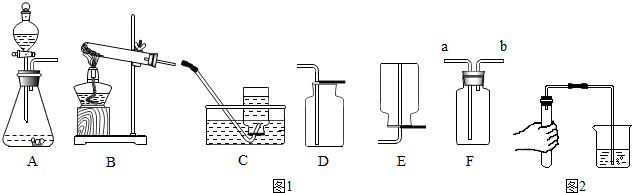
(1)甲同学用氯酸钾和二氧化锰共热制备和收集氧气,他应选用的气体发生装置是(填序号).他用装置C来收集的原因是,当看到导管口的时他才开始收集氧气.
(2)该同学用如图2所示的方法进行气密性检查,如果装置不漏气,可以看到,将手松开一段时间后(导管仍插入水中),可以看到导管中会形成一段水柱.
(3)因为氧气的密度比空气的稍大,所以还可以选用(填序号)来收集氧气,其验满的方法是.
(4)老师提醒可以用F(万能瓶)来收集气体,则甲同学应将发生装置的导管与F的导管(选填a或b)相连接.
(5)乙同学称取一定质量的KMnO4固体放入大试管中,将温度控制在250℃加热制取O2.实验结束时,这位同学发现用排水法收集到的O2大于理论产量.针对这一现象,同学们进行了如下探究:
【提出猜想】猜想Ⅰ:反应生成的二氧化锰(MnO2)分解放出O2;
猜想Ⅱ:反应生成的锰酸钾(K2MnO4)分解放出O2;
【实验验证】同学们分成两组,分别进行下列实验:
第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变,则猜想(选填Ⅰ或Ⅱ)错误;
第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论.该组同学选择的实验方法是.
【拓展延伸】实验发现,KClO3固体加热制取O2的反应速率很慢,但如果将KMnO4固体与KClO3固体混合加热,则KClO3的分解速率大大加快,请说明KMnO4在KClO3的分解反应中是否作催化剂,为什么?.
(6)丙同学选择用双氧水和二氧化锰混合来制氧气,则他应选用的气体发生装置是(填序号).以下是他探究影响该反应速率因素的相关实验数据.
通过以上实验数据的分析,可知,过氧化氢分解制氧气的化学反应速率与实验
序号H2O2溶液浓度% H2O2溶液体积/mL 温度℃ MnO2用量/g 收集到的
氧气体积/mL反应所需的
时间/s① 5 1 20 1 30.29 ② 5 1 20 0.1 4 16.75 ③ 15 1 20 0.1 4 6.04 ④ 30 1 55 2 10.76 、、等因素有关;发生装置中的(填仪器名称)也可以帮助控制反应的速率.发布:2024/12/18 8:0:1组卷:12引用:2难度:0.5 -
3.下列探究影响化学反应速率因素的实验中,实验方案正确的是( )
选项 影响因素 实验方案 A 接触面积 将1g块状石灰石和20mL10%的稀盐酸、1g粉末状石灰石与20mL10%的稀硫酸混合,比较产生气泡的快慢 B 催化剂的种类 将0.5g二氧化锰、1g氧化铁分别与10mL6%的过氧化氢溶液混合,比较产生气泡的快慢 C 反应物的种类 分别将木炭在空气中、氧气中燃烧,比较反应的剧烈程度 D 反应物的性质 分别用酒精灯加热表面积相同的镁片和铁片,比较在空气中能否被点燃 发布:2024/12/25 13:0:1组卷:114引用:4难度:0.7


