海带中含有碘元素,从海带中提取碘的实验过程如图所示。
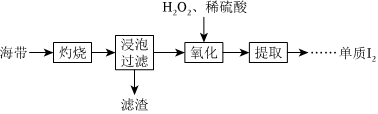
(1)“灼烧”时用到下列仪器中的 ADAD。
A.酒精灯
B.漏斗
C.蒸发皿
D.坩埚
(2)“浸泡过滤”后滤液中含有I-,“氧化”的离子方程式为 2I-+H2O2+2H+=I2+2H2O2I-+H2O2+2H+=I2+2H2O。
(3)检验“氧化”产生I2的操作:取“氧化”后的少量溶液于试管中,向溶液中滴加几滴淀粉溶液,溶液变蓝向溶液中滴加几滴淀粉溶液,溶液变蓝(实验操作及现象)。
(4)“提取”存在以下两种方案。
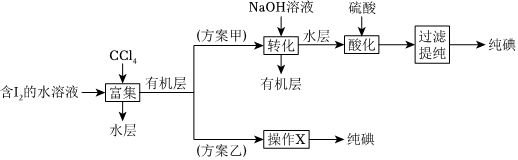
已知:3I2+6NaOH=5NaI+NaIO3+3H2O;酸性条件下,I2在水溶液中的溶解度很小。
①方案乙中“操作X”的名称是 蒸馏蒸馏。
②方案甲中,“酸化”步骤氧化剂与还原剂物质的量之比为 1:51:5。
③该流程可循环利用的物质是 CCl4CCl4。
④采用方案乙得到纯碘的产率较低,原因是 碘易升华,达到四氯化碳的沸点时,大多数碘会随着四氯化碳一起蒸出碘易升华,达到四氯化碳的沸点时,大多数碘会随着四氯化碳一起蒸出。
【考点】从海带中提取碘.
【答案】AD;2I-+H2O2+2H+=I2+2H2O;向溶液中滴加几滴淀粉溶液,溶液变蓝;蒸馏;1:5;CCl4;碘易升华,达到四氯化碳的沸点时,大多数碘会随着四氯化碳一起蒸出
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/8/31 0:0:8组卷:64引用:1难度:0.5
相似题
-
1.下列物质的工业制备方案合理的是( )
发布:2024/12/21 8:0:2组卷:24引用:1难度:0.5 -
2.海带中含有丰富的碘元素(以I-形式存在)。实验中提取碘的流程如图:
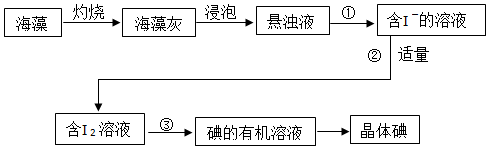
(1)①写出氯原子的原子结构示意图: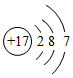
②写出I-的电子式:
③写出步骤②发生的离子方程式
(2)①实验①的操作名称
②实验③所需要的主要玻璃仪器为、烧杯。
(3)①实验操作③中,(填“能”或“不能”)用酒精来提取碘。
②实验操作③中,若用苯来提取碘,加入少量苯,充分振荡静置后的现象是。
A.溶液分层,下层红棕色
B.溶液分层,上层红棕色
C.溶液分层,下层紫红色
D.溶液分层,上层紫红色
(4)检验某无色溶液中是否含有I-,所用试剂不合理的是。
A.淀粉溶液和氯水
B.稀硝酸和硝酸银溶液
C.氯水和四氯化碳
D.KBr和稀HCl
(5)下列有关从海带中提取碘的实验原理和装置能达到实验目的是
A.用装置甲灼烧碎海带
B.用装置乙过滤海带灰的浸泡液
C.用装置丙制备用于氧化浸泡液中I-的Cl2
D.用装置丁吸收氧化浸泡液中I-后的Cl2尾气发布:2024/12/30 8:30:1组卷:56引用:2难度:0.7 -
3.海洋植物如海带、海藻中含有丰富的碘元素。碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如图:
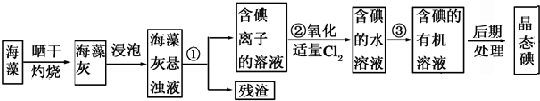
(1)指出制取碘的过程中有关的实验操作名称:①。②。
(2)提取碘的过程中。可供选择的有机试剂是。
A.甲苯、酒精 B.四氯化碳、苯 C.汽油、乙酸 D.汽油、甘油
(3)为使海藻灰中碘离子转化为碘的有机溶液。实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品。尚缺少的玻璃仪器是。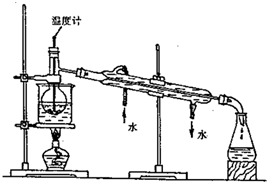
(4)从含碘的有机溶液中提取碘和回收有机溶液。还需要经过蒸馏。观察右图实验装置指出其错误之处。;;(任意说两点即可)
(5)已知常压下碘的升华温度137.2℃,四氯化碳沸点77℃.进行上述蒸馏操作时。使用水浴的原因是。最后晶态碘在里聚集。发布:2024/12/30 13:30:2组卷:89引用:3难度:0.5


