回答下列问题:
Ⅰ、某NaCl溶液中混有Na2SO4、Na2CO3溶液和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如图:
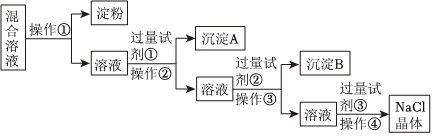
(1)写出上述实验过程中所用试剂(填化学式)和基本实验操作:试剂②Na2CO3Na2CO3;试剂③HClHCl;操作①渗析渗析;操作④蒸发结晶蒸发结晶。
(2)区分淀粉胶体和NaCl溶液的方法是:丁达尔效应丁达尔效应。
(3)沉淀B为 BaCO3BaCO3。
(4)加入试剂①产生沉淀的离子方程式:Ba2++SO2-4=BaSO4↓Ba2++SO2-4=BaSO4↓,Ba2++CO2-3=BaCO3↓Ba2++CO2-3=BaCO3↓。
(5)操作①是利用半透膜进行分离提纯。操作①的实验结果:淀粉 不能不能透过半透膜。(填“能”或者“不能”)
Ⅱ、一份无色透明溶液中可能含有K+、Na+、Fe3+、H+、CO2-3、HCO-3、Cl-离子中的若干种,且离子个数相等。为了确定溶液的组成,进行了如下操作:
①取2mL溶液,加足量稀盐酸,产生无色无味气体,该气体能使澄清石灰水变浑浊。
②取2mL溶液,先加足量稀硝酸酸化,有气体产生,再加硝酸银溶液进行检验,有白色沉淀产生。
(6)原溶液中一定不存在的阴离子是 CO2-3CO2-3,原溶液中一定存在的阳离子是 Na+、K+Na+、K+。
(7)向该透明溶液中加入NaOH溶液,是否有反应发生?若没有,填“否”;若有,请写出有关的离子方程式 OH-+HCO-3=CO2-3+H2OOH-+HCO-3=CO2-3+H2O。
SO
2
-
4
SO
2
-
4
CO
2
-
3
CO
2
-
3
CO
2
-
3
HCO
-
3
CO
2
-
3
CO
2
-
3
HCO
-
3
CO
2
-
3
HCO
-
3
CO
2
-
3
【答案】Na2CO3;HCl;渗析;蒸发结晶;丁达尔效应;BaCO3;Ba2++=BaSO4↓;Ba2++=BaCO3↓;不能;;Na+、K+;OH-+=+H2O
SO
2
-
4
CO
2
-
3
CO
2
-
3
HCO
-
3
CO
2
-
3
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/7/25 8:0:9组卷:19引用:2难度:0.7
相似题
-
1.化学家从反应C2H6(g)+Cl2(g)→C2H5Cl(l)+HCl(g)中受到启发,提出在农药和有机合成工业中可获得副产品盐酸,这一设想已成为现实.试指出从上述反应体系中得到盐酸可采用的分离方法是( )
发布:2024/12/30 9:30:2组卷:25引用:3难度:0.9 -
2.分离乙酸乙酯、乙醇、乙酸的混合物,可按下列步骤进行:
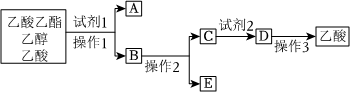
(1)试剂1最好选用。
(2)操作1是,所用的主要仪器名称是。
(3)操作2是。
(4)试剂2最好选用。
(5)有同学认为乙酸在温度低于16.6℃时会凝结成晶体,因此可通过降温的方法使乙酸结晶而分离出来,操作3是结晶、过滤,这一看法是否正确?为什么?发布:2024/12/30 14:30:1组卷:15引用:5难度:0.4 -
3.苯甲酸的重结晶实验基本操作如下:
①将粗苯甲酸1g加到100mL的烧杯中,再加入50mL蒸馏水,在石棉网上边搅拌边加热,使粗苯甲酸溶解,②全溶后再加入少量蒸馏水并搅拌.③然后,使用短颈玻璃漏斗趁热将溶液过滤到另一100mL烧杯中,将滤液静置,使其缓慢冷却结晶.④滤出晶体.回答下列问题:
(1)上述四步操作过程中需用到玻璃棒的步骤有
(2)步骤②的目的是;
(3)观察滤液冷却时的实验现象:;
(4)重结晶后苯甲酸的状态:.发布:2024/12/30 8:30:1组卷:45引用:4难度:0.5


