同学们往盛有NaOH溶液的试管中通入CO2,未看到明显现象,于是对NaOH与CO2是否发生反应进行了探究和拓展实验。

活动一:
(1)甲同学设计了如图1所示实验(装置气密性良好),观察到的实验现象为 塑料瓶变瘪塑料瓶变瘪。
(2)甲同学认为上述实验操作及现象足以证明氢氧化钠与二氧化碳发生了反应,其他同学均认为不合理,理由是 二氧化碳能溶于水、且能与水反应也会使塑料瓶变瘪二氧化碳能溶于水、且能与水反应也会使塑料瓶变瘪。
活动二:
(3)取活动一结束后软塑料瓶中的液体于三支试管中,分别进行如图2所示实验。当观察到三支试管中有明显现象时,均证明氢氧化钠和二氧化碳发生了反应。A、B、C试管中的现象分别为 试管A中产生气泡,试管B中产生白色沉淀,试管C中产生白色沉淀试管A中产生气泡,试管B中产生白色沉淀,试管C中产生白色沉淀,试管中反应的化学反应方程式为 2HCl+Na2CO3=2NaCl+CO2↑+H2O或CaCl2+Na2CO3=2NaCl+CaCO3↓或Ca(OH)2+Na2CO3=2NaOH+CaCO3↓2HCl+Na2CO3=2NaCl+CO2↑+H2O或CaCl2+Na2CO3=2NaCl+CaCO3↓或Ca(OH)2+Na2CO3=2NaOH+CaCO3↓(任写其一)。
活动三:活动二结束后,同学们将三支试管中的剩余物倒入一个洁净的大烧杯中进行废液回收,搅拌静置后发现烧杯内上层为无色清液,下层有白色沉淀,如图3。
(4)上层清液中一定不会大量存在的离子是 氢离子氢离子。
(5)为检验上层清液中是否存在大量OH-和CO2-3,同学们按下列表格进行试验,请完善表格。
CO
2
-
3
| 实验步骤 | 实验现象 | 实验结论 |
| ①取烧杯中上层清液少许于试管中,滴加Ba(NO3)2溶液 | 无明显现象 |
没有碳酸根离子 没有碳酸根离子
|
| ②另取烧杯中上层清液少许于试管中,滴加 氯化铜溶液 氯化铜溶液 (指示剂除外) |
产生蓝色沉淀 产生蓝色沉淀
|
有大量OH- |
查阅文献得知:无水CaCl2只吸收水而不吸收二氧化碳。
(6)①盛装药品后,称得总质量为m1。
②逐滴加入稀硫酸至不再产生气泡。待电子天平读数不再改变时,称得总质量为m2。同学们将(m1-m2)作为CO2质量,计算碳酸钠的质量分数,你认为计算得到的值与真实值比较
偏小
偏小
(填“偏大”、“偏小”或“不变”),理由是 残留在锥形瓶内的二氧化碳没有完全排出,导致(m1-m2)偏小,进一步导致实验结果偏小
残留在锥形瓶内的二氧化碳没有完全排出,导致(m1-m2)偏小,进一步导致实验结果偏小
。【答案】塑料瓶变瘪;二氧化碳能溶于水、且能与水反应也会使塑料瓶变瘪;试管A中产生气泡,试管B中产生白色沉淀,试管C中产生白色沉淀;2HCl+Na2CO3=2NaCl+CO2↑+H2O或CaCl2+Na2CO3=2NaCl+CaCO3↓或Ca(OH)2+Na2CO3=2NaOH+CaCO3↓;氢离子;没有碳酸根离子;氯化铜溶液;产生蓝色沉淀;偏小;残留在锥形瓶内的二氧化碳没有完全排出,导致(m1-m2)偏小,进一步导致实验结果偏小
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/8/7 8:0:9组卷:86引用:2难度:0.4
相似题
-
1.化学兴趣小组的同学在进行酸和碱的性质探究时,进行了图一、图二、图三等三个实验:
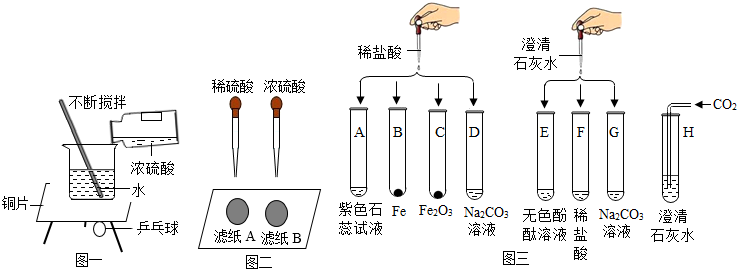
(1)【实验一】浓硫酸稀释过程中的能量变化。
图一实验中,观察到用石蜡固定在铜片下的乒乓球脱落,说明浓硫酸稀释时(填“吸热”或“放热”)
(2)【实验二】溶液浓度对硫酸化学性质的影响。
图二实验中,观察到很快变黑的是滤纸(填“A”或“B”),由此可知,硫酸溶液的浓度不同,性质不同。
(3)【实验三】探究盐酸和氢氧化钙的化学性质,取8支试管分别用A-H编号后,做如图三的实验。
①实验中观察到有气泡生成的试管是(填编号);
②试管C中反应的化学方程式为。
③实验后某试管中为红色溶液,当向其中加入过量的澄清石灰水后,溶液变为蓝色。由此推断,该试管是。(填编号)
④H试管的反应常用来检验二氧化碳,请写出反应的化学方程式。
⑤E、F、G试管实验完成后,将试管内清液都倒入同一只洁净的大烧杯中,发现有白色沉淀生成,上层清液呈无色。上层清液中溶质的成分除酚酞外一定有,可能还有。发布:2024/12/25 12:0:1组卷:96引用:5难度:0.5 -
2.某化学兴趣小组的同学利用实验室器材进行了实验探究

[实验一]如图1是实验室常用的几种实验装置,请回答下列问题:
(1)写出实验室用AE装置组合制取某种气体的化学方程式,用E装置收集该气体,气体从(填“a”或“b”)端进入。
(2)实验室制取的CO2中常含有少量杂质气体会干扰F实验的目的。为排除干扰,除去该杂质并检验是否除净,将产生的混合气体依次通过上述装置(在B至E中选择,填序号,装置不重复),再进入F装置:F装置内产生的现象为。
[实验二]探究酸碱中和反应。利用图2装置进行实验,实验开始后将注射器内的液体逐滴注入烧瓶内。
(1)实验测得烧杯中溶液的pH随时间的变化关系如图3所示,c点所示溶液加热蒸干所得固体是(填化学式)。
(2)该反应是放热反应,对应图3中点温度最高。
(3)能说明盐酸和氢氧化钠发生化学反应的依据是:
①溶液的颜色从红色变为无色;②溶液的pH。
[实验三]探究NaOH和CO2的反应。
(1)从压强变化的角度探究。
①利用图4装置进行实验,先挤压胶头滴管,再打开止水夹,观察到烧瓶内形成红色“喷泉”,原因是烧瓶内压强(填“大于”或“小于”)外界大气压;
②利用图5装置进行实验,分别将等体积的NaOH溶液和水同时注入盛有等体积CO2的玻璃容器中。证明CO2与NaOH溶液发生反应的实验现象是。
(2)利用“数字化实验”探究。利用图6装置进行实验,实验过程中装置内压强变化如图7所示,a点时推入NaOH溶液,b点时推入稀盐酸。
①ab段对应反应的化学方程式;
②bc段压强不变的原因是;
③证明CO2与NaOH溶液发生反应的实验现象是。发布:2024/12/25 16:30:1组卷:156引用:2难度:0.3 -
3.在实验课上,同学们将CO2通入到Ca(OH)2溶液中观察到有白色沉淀生成,而将CO2通入到NaOH溶液中无明显现象。
【提出问题】CO2与NaOH溶液是否发生了化学反应?
【提出猜想】CO2与NaOH溶液发生了化学反应
【实验探究】小明设计出了下列4种实验装置,其共同原理是二氧化碳和氢氧化钠溶液反应,使容器内压强降低。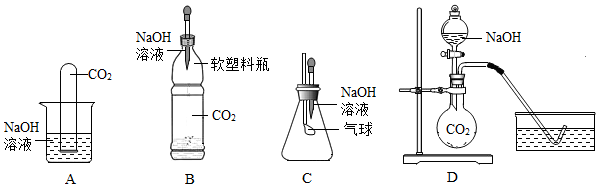
(1)实验现象为:A中试管内液面上升,B中,C中,D中水槽中的水部分进入烧瓶。
(2)小宁对小明的方案提出了质疑,他认为小明的实验不严谨,其理由是要得到科学严谨的结论,利用方案A,补做的对比实验是。
(3)小丽的改进方案是利用反应后的溶液来验证猜想,请完成实验报告。
【得出结论】CO2与NaOH溶液发生了化学反应,请写出CO2与NaOH反应的化学方程式:实验操作 实验现象 实验结论 向实验后的溶液
中加入稀盐酸猜想正确 。发布:2024/12/25 11:0:2组卷:73引用:3难度:0.1
相关试卷


