气体的制取是初中化学的重要内容。学校兴趣小组同学进行实验研究。
【活动一】研究氧气的制取

(1)写出有标号的仪器名称:①酒精灯酒精灯。
(2)实验室用高锰酸钾制氧气选用的发生装置是 AA(填图1字母),反应的化学方程式为 2KMnO4 △ K2MnO4+MnO2+O2↑2KMnO4 △ K2MnO4+MnO2+O2↑,用图D装置收集的氧气,判断收集满了的方法是 瓶口有大气泡逸出瓶口有大气泡逸出。
(3)化学兴趣小组同学根据所学知识,自制一台“制氧器”,其装置如图3所示。该装置使用甲试剂为白色固体(Na2CO3•3H2O2),作制氧剂;乙试剂为二氧化锰,作催化剂。该制氧机的制氧原理有两步:
第一步:Na2CO3•3H2O2 40℃ Na2CO3+3H2O2
第二步:2H2O2 MnO2 2H2O+O2↑2H2O2 MnO2 2H2O+O2↑(用化学方程式表示)。
由上述资料信息可知,保存Na2CO3•3H2O2应注意 放在阴凉干燥处放在阴凉干燥处。
下列有关该装置说法正确的是 BCBC(填字母)。
A.此仪器可用于医疗急救,也可用产生的氧气作燃料切割金属
B.过滤仓利用氧气不易溶于水的性质,使氧气湿润
C.过滤仓中气泡的多少可以判断氧气排出的快慢
D.该装置可以随时调控产生氧气的速率
【活动二】研究二氧化碳的制取
(4)按如下表进行实验,取等质量的同种大理石加入足量酸中(杂质不与酸反应),产生二氧化碳的体积随时间变化曲线如图4所示。
△
△
40
℃
M
n
O
2
M
n
O
2
| 实验编号 | 药品 |
| Ⅰ | 块状大理石、10%稀硫酸 |
| Ⅱ | 块状大理石、7%稀盐酸 |
| Ⅲ | 粉状大理石、7%稀盐酸 |
丙
丙
(选填“甲”、“乙”或“丙”)。小组同学决定用实验Ⅱ的药品制取二氧化碳气体,不用实验Ⅲ药品制备二氧化碳的原因是 粉状大理石与稀盐酸接触面积大,反应速率太快
粉状大理石与稀盐酸接触面积大,反应速率太快
。(5)实验小组同学在制取二氧化碳时想要控制反应的发生和停止,应选择图1中的
C
C
作发生装置。选择图2为收集装置,检验二氧化碳已收集满的方法为 将燃着的木条伸到b端导管口,木条熄灭,证明已收集满
将燃着的木条伸到b端导管口,木条熄灭,证明已收集满
。(6)小明同学将25g鸡蛋壳(鸡蛋壳的主要成分是碳酸钙)洗净、干燥并捣碎后放入锥形瓶里,加入足量的稀盐酸充分反应(假设其他杂质不与盐酸反应),收集到8.8g气体。请帮小明计算鸡蛋壳中碳酸钙的质量分数
80%
80%
。【答案】酒精灯;A;2KMnO4 K2MnO4+MnO2+O2↑;瓶口有大气泡逸出;2H2O2 2H2O+O2↑;放在阴凉干燥处;BC;丙;粉状大理石与稀盐酸接触面积大,反应速率太快;C;将燃着的木条伸到b端导管口,木条熄灭,证明已收集满;80%
△
M
n
O
2
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/24 20:0:2组卷:57引用:1难度:0.5
相似题
-
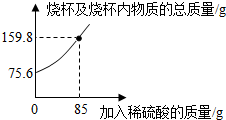 1.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为52.2g的烧杯中,然后缓慢加入一定质量的稀硫酸,当加稀硫酸质量为85g时,反应恰好完全(杂质不反应且产生的气体全部逸出),反应过程中的质量关系如图.完成下列问题:
1.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为52.2g的烧杯中,然后缓慢加入一定质量的稀硫酸,当加稀硫酸质量为85g时,反应恰好完全(杂质不反应且产生的气体全部逸出),反应过程中的质量关系如图.完成下列问题:
(1)该实验取用的样品质量为g.
(2)计算样品中铁的质量分数(写出解题过程).发布:2025/1/9 8:0:2组卷:139引用:39难度:0.1 -
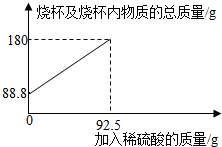 2.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为51.8克的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入92.5g稀硫酸时恰好完全反应,加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图。
2.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为51.8克的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入92.5g稀硫酸时恰好完全反应,加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图。
(1)该实验取用的样品质量为g。
(2)反应后所得溶液中的溶质的质量分数。(写出计算过程,结果保留一位小数)
(3)反应结束后,小明不慎向烧杯中多加了10g稀硫酸,若在图中补绘此过程中稀硫酸的质量与烧杯及烧杯内物质的总质量的关系图,所得线段的终点位于线段AB延长线的(填:上方、下方或线上)。发布:2025/1/9 8:0:2组卷:4引用:1难度:0.3 -
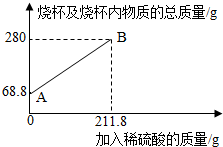 3.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为51.8克的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入211.8g稀硫酸时恰好完全反应,加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图。
3.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为51.8克的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入211.8g稀硫酸时恰好完全反应,加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图。
(1)该实验取用的样品质量为g。
(2)求样品中铁的质量分数;反应后所得溶液中的溶质的质量分数。(写出计算过程,结果保留一位小数)
(3)反应结束后,小明不慎向烧杯中多加了20g稀硫酸,若在图中补绘此过程中稀硫酸的质量与烧杯及烧杯内物质的总质量的关系图,所得线段的终点位于线段AB延长线的(填:上方、下方或线上)。发布:2025/1/9 8:0:2组卷:8引用:1难度:0.3


