天然气中含有的H2S会腐蚀管道设备,开采天然气后须及时除去H2S。在此过程中会产生大量含硫废水(其中硫元素的主要化合价是-2价),对设备、环境等边成严重危害。
已知:ⅰ:H2S有剧毒;常温下溶解度为1:2.6(体积)。
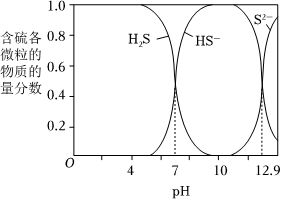
ⅱ:H2S、HS-、S2-在水溶液中的物质的量分数随pH的分布曲线如图。
ⅲ:碳酸的电离平衡常数:Ka1=4.5×10-7,Ka2=4.7×10-11
(1)用过量的Na2CO3溶液吸收天然气中的H2S的离子方程式是 H2S+CO2-3⇌HCO-3+HS-H2S+CO2-3⇌HCO-3+HS-,该反应对应的化学平衡常数K=10-74.7×10-11≈2.13×10310-74.7×10-11≈2.13×103(列出计算式)。
(2)①当pH≈8时,含硫废水中H2S、HS-的浓度比是 1:101:10。
②NaHS溶液呈碱性,原因是 HS-水解平衡常数Kh=KwKa1(H2S)=10-1410-7=10-7>Ka2=10-12.9,可知水解程度大于电离程度,则水解生成的c(OH-)>c(H+),溶液呈碱性HS-水解平衡常数Kh=KwKa1(H2S)=10-1410-7=10-7>Ka2=10-12.9,可知水解程度大于电离程度,则水解生成的c(OH-)>c(H+),溶液呈碱性(结合化学用语说明)。
(3)沉淀法处理含硫废水:
向pH≈9的含硫废水中加入适量Cu2+的溶液,观察到有黑色沉淀生成,则溶液的pH 降低降低(填“升高”“降低”或“不变”)。用化学平衡移动的原理解释产生上述现象的原因:废水中存在水解平衡:S2-+H2O⇌HS-+OH-,加入适量Cu2+的溶液,发生反应:Cu2++S2-=CuS↓,生成黑色CuS沉淀;S2-浓度减小,水解平衡逆向移动,导致c(OH-)减小,pH值降低废水中存在水解平衡:S2-+H2O⇌HS-+OH-,加入适量Cu2+的溶液,发生反应:Cu2++S2-=CuS↓,生成黑色CuS沉淀;S2-浓度减小,水解平衡逆向移动,导致c(OH-)减小,pH值降低。
(4)氧化还原法处理含硫废水:
向pH≈9的含硫废水中加入一定浓度的Na2SO3溶液,加酸将溶液调为pH=5,产生淡黄色沉淀。
①反应的离子方程式是 2S2-+SO2-3+6H+=3S↓+3H2O2S2-+SO2-3+6H+=3S↓+3H2O。
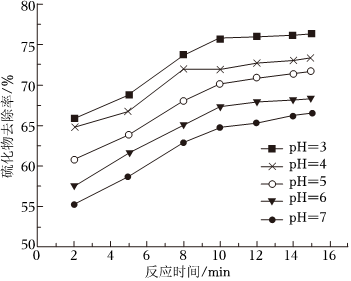
②不同pH时,硫化物去除率随时间的变化曲线如图所示。本工艺选择控制体系的pH=5,不选择pH<5,从环境保护的角度分析其主要原因:pH<5时,溶液中-2价S元素主要以H2S的形式存在,常温下H2S的溶解度为1:2.6,酸性强使H2S更易逸出,H2S有剧毒会污染环境pH<5时,溶液中-2价S元素主要以H2S的形式存在,常温下H2S的溶解度为1:2.6,酸性强使H2S更易逸出,H2S有剧毒会污染环境。
H
2
S
+
C
O
2
-
3
⇌
HC
O
-
3
+
H
S
-
H
2
S
+
C
O
2
-
3
⇌
HC
O
-
3
+
H
S
-
1
0
-
7
4
.
7
×
1
0
-
11
≈
2
.
13
×
1
0
3
1
0
-
7
4
.
7
×
1
0
-
11
≈
2
.
13
×
1
0
3
K
w
K
a
1
(
H
2
S
)
=
1
0
-
14
1
0
-
7
=
1
0
-
7
K
a
2
=
1
0
-
12
.
9
K
w
K
a
1
(
H
2
S
)
=
1
0
-
14
1
0
-
7
=
1
0
-
7
K
a
2
=
1
0
-
12
.
9
S
2
-
+
H
2
O
⇌
H
S
-
+
O
H
-
S
2
-
+
H
2
O
⇌
H
S
-
+
O
H
-
2
S
2
-
+
S
O
2
-
3
+
6
H
+
=
3
S
↓
+
3
H
2
O
2
S
2
-
+
S
O
2
-
3
+
6
H
+
=
3
S
↓
+
3
H
2
O
【答案】;;1:10;HS-水解平衡常数Kh=>,可知水解程度大于电离程度,则水解生成的c(OH-)>c(H+),溶液呈碱性;降低;废水中存在水解平衡:,加入适量Cu2+的溶液,发生反应:Cu2++S2-=CuS↓,生成黑色CuS沉淀;S2-浓度减小,水解平衡逆向移动,导致c(OH-)减小,pH值降低;;pH<5时,溶液中-2价S元素主要以H2S的形式存在,常温下H2S的溶解度为1:2.6,酸性强使H2S更易逸出,H2S有剧毒会污染环境
H
2
S
+
C
O
2
-
3
⇌
HC
O
-
3
+
H
S
-
1
0
-
7
4
.
7
×
1
0
-
11
≈
2
.
13
×
1
0
3
K
w
K
a
1
(
H
2
S
)
=
1
0
-
14
1
0
-
7
=
1
0
-
7
K
a
2
=
1
0
-
12
.
9
S
2
-
+
H
2
O
⇌
H
S
-
+
O
H
-
2
S
2
-
+
S
O
2
-
3
+
6
H
+
=
3
S
↓
+
3
H
2
O
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/13 3:0:1组卷:51引用:3难度:0.5


