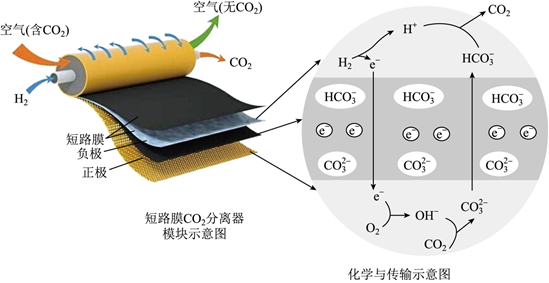
汽车尾气中氮氧化合物、碳氧化合物的处理与利用是各国研究的热点。
(1)已知断裂1molN≡N、H-H、N-H分别需要吸收945kJ、436kJ、391kJ的能量,在一定条件下消耗了1molN2和3molH2生成2molNH3,该过程会 释放释放(填“吸收”或“释放”) 9393kJ的能量。
(2)汽车排气管内安装的催化转化器可处理尾气的主要污染物(NO和CO),发生反应:2NO(g)+2CO(g)⇌2CO2(g)+N2(g)。某实验小组在200℃、5L恒容密闭容器中充入等物质的量的CO与NO模拟该过程,NO的物质的量随时间变化如表所示。
| t/s | 0 | 10 | 20 | 30 | 40 | 50 |
| n(NO)/mol | 0.40 | 0.35 | 0.31 | 0.30 | 0.30 | 0.30 |
BC
BC
(填序号)。A.反应速率:v(NO)=v(CO)
B.混合气体的压强不再改变
C.混合气体中NO的物质的量分数保持不变
D.混合气体的密度不再改变
②10s~20s内用N2表示该反应的平均反应速率为
0.0004mol/(L•s)
0.0004mol/(L•s)
。③该条件下,CO的最大转化率为
25%
25%
。④下列措施一定能增大该反应速率的是
AC
AC
(填序号)。A.适当升高温度
B.充入Ne
C.适当减小容器的容积
D.及时分离出CO2、N2
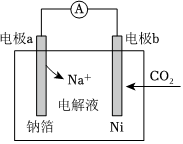
(3)CO2是一种能引起温室效应的气体,有一种室温下“可呼吸”的Na-CO2电池装置可吸收一定量的CO2,装置如图所示,电池的总反应为3CO2+4Na=2Na2CO3+C。
①电极a为
负
负
极(填“正”或“负”)。②电极b发生的电极反应为
3CO2+4e-═2+C
CO
2
-
3
3CO2+4e-═2+C
。CO
2
-
3
【答案】释放;93;BC;0.0004mol/(L•s);25%;AC;负;3CO2+4e-═2+C
CO
2
-
3
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/8/1 8:0:9组卷:24引用:1难度:0.6