 海洋可谓地球的“聚宝盆”,蕴藏着极为丰富的化学资源,如海水中就有80多种元素,氯化物的含量很高。其中,Br和I在陆地上的含量较少,主要是从海洋中提取。
海洋可谓地球的“聚宝盆”,蕴藏着极为丰富的化学资源,如海水中就有80多种元素,氯化物的含量很高。其中,Br和I在陆地上的含量较少,主要是从海洋中提取。
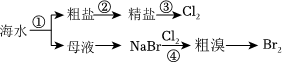
(1)如图所示为海水综合利用部分流程,有关说法不正确的是 CC。
A.实验室进行①的操作需用到得玻璃仪器有漏斗、玻璃棒、烧杯
B.②步中加入试剂的顺序可以是BaCl2溶液→Na2CO3溶液→NaOH溶液→过滤后盐酸
C.①②③④反应都涉及氧化还原反应
D.④步得到的粗品进行提纯时鼓入热空气是为了利用Br2易挥发的性质
(2)设NA为阿伏加德罗常数的值。下列叙述正确的是 DD。
A.1molNH4Cl含有的共价键数目为5NA
B.1molNaHCO3完全分解,得到的CO2分子数目为NA
C.标准状况下,11.2L氯气通入水中,溶液中Cl-和ClO-离子数之和为NA
D.NaBr和NH4Br的混合物中含1molBr-,则混合物中质子数目为46NA
(3)已知HCl还常用于聚氯乙烯的制备,试写出聚氯乙烯的链节:
 。
。
常用的消毒剂有双氧水、医用酒精以及含氯消毒剂。其中含氯消毒剂的家族最庞大、应用最广泛,其中又以“84消毒液”(有效成分为NaClO)最为人所熟知。
(4)生活中,84消毒液是一种常用消毒剂,用化学方程式表示其生效原理为 NaClO+CO2+H2O=HClO+NaHCO3NaClO+CO2+H2O=HClO+NaHCO3。
(5)ClO2是一种新型的高效消毒剂。工业上常用下法制备ClO2(其中HCl起酸性和还原性):
22NaClO3+44HCl═2ClO2+11Cl2+2H2O2H2O+2NaCl
配平上述反应方程式并用单线桥表示电子转移的方向和数目 
 。
。
(6)已知SnCl2易水解,实验室利用SnCl2•2H2O固体配制490mL1mol•L-1SnCl2溶液。下列说法正确的是 CDCD(双选)
A.配制溶液时490mL容量瓶需要干燥
B.配制溶液过程中,玻璃棒只起到引流的作用
C.需用电子天平称量112.850gSnCl2•2H2O固体
D.溶解SnCl2•2H2O固体时需要用盐酸代替蒸馏水




【答案】C;D; ;NaClO+CO2+H2O=HClO+NaHCO3;2;4;1;2H2O;
;NaClO+CO2+H2O=HClO+NaHCO3;2;4;1;2H2O; ;CD
;CD
 ;NaClO+CO2+H2O=HClO+NaHCO3;2;4;1;2H2O;
;NaClO+CO2+H2O=HClO+NaHCO3;2;4;1;2H2O; ;CD
;CD【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/18 1:0:1组卷:19引用:1难度:0.6
相似题
-
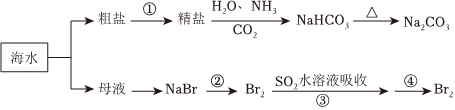
1.海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。下列有关说法不正确的是( )
 发布:2024/12/30 3:30:1组卷:129引用:9难度:0.6
发布:2024/12/30 3:30:1组卷:129引用:9难度:0.6 -
2.海水是化学元素的宝库,从海水中可以提取或生产多种化工原料,如食盐、氯气、单质溴、镁、纯碱等,它们在工农业生产中有着广泛的用途.根据学过的知识回答下列问题:
(1)某化学兴趣小组计划用氯气和氢氧化钠制取简易消毒液.
①其反应原理为:(用离子方程式表示).
②配制250mL 4.0mol•L-1NaOH溶液,需要用到的玻璃仪器,除烧杯、玻璃棒外,还必须用到的是.
(2)工业制得粗硅后,再与氯气等物质发生反应,最终得到纯硅.请写出工业制取粗硅的化学方程式:
(3)金属镁被誉为“国防金属”,若镁起火,不能用CO2来灭火,其原因可用化学方程式表示为
(4)①若Na2CO3固体中混有少量NaHCO3杂质,除去杂质的方法是,
②若NaHCO3溶液中混有少量Na2CO3杂质,除去杂质的方法是.发布:2024/10/27 17:0:2组卷:11引用:1难度:0.5 -
3.海水资源开发利用的部分过程如图所示:
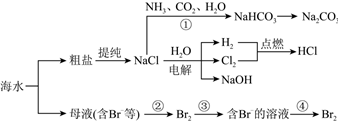
下列说法正确的是( )发布:2024/11/3 6:0:1组卷:51引用:3难度:0.7


