实验室为制备和收集少量干燥、纯净的氯气,选用如图所示仪器及药品:

(1)上述实验中,用来盛放浓盐酸的仪器的名称是 分液漏斗分液漏斗。
(2)制取氯气的离子反应方程式为 MnO2+4H++2Cl- △ Mn2++Cl2↑+2H2OMnO2+4H++2Cl- △ Mn2++Cl2↑+2H2O。
(3)选择上述仪器并按顺序连接(填各接口处的字母):a→d→f→b→cd→f→b→c→k→i→h。
(4)如图是一组探究氯气性质的装置。

现关闭活塞K,若有色布条是干燥的,溶液A为浓硫酸,则有色布条 不褪色不褪色(填现象,下同)。
(5)现打开K,溶液A为氢氧化钠溶液,通入的氯气是湿润的,布条是干燥的,则有色布条 褪色褪色。
(6)使用氯气消毒易产生危害人体健康的有机氯化物。用氯气和亚氯酸钠(NaClO2)溶液可制备新的绿色消毒剂二氧化氯(ClO2),反应中还可得到氯化钠。该反应的化学方程式为 Cl2+2NaClO2=2ClO2+2NaClCl2+2NaClO2=2ClO2+2NaCl。
(7)若用含0.2molHCl的浓盐酸与足量的MnO2反应制取Cl2,制得Cl2体积 <<(填“>”“<”或“=”)1.12L(标准状况)。
△
△
【答案】分液漏斗;MnO2+4H++2Cl- Mn2++Cl2↑+2H2O;d→f→b→c;不褪色;褪色;Cl2+2NaClO2=2ClO2+2NaCl;<
△
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/20 3:0:2组卷:22引用:2难度:0.5
相似题
-
1.为了验证干燥的氯气无漂白性,湿润的氯气具有漂白性,某同学设计实验如图.其中B、C、D、E、F分别盛有饱和食盐水、浓硫酸.干燥红色布条、浓硫酸、湿润红色布条.
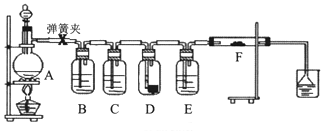
请回答:
(1)E中浓硫酸的作用.
(2)将F中的湿润布条换成卷曲的细铜丝,并用酒精灯加热,可看到的现象是.
(3)若用装置A制取2.24L(标况)氯气,消耗10mol/L浓盐酸的体积明显大于40mL,造成该结果的可能原因有.
A.浓盐酸的挥发 B.随反应进行盐酸浓度下降
C.加热时火力不够猛 D.MnO2固体过量.发布:2025/1/15 8:0:2组卷:17引用:1难度:0.3 -
2.如图是某同学设计的氯气制备及性质验证实验装置。相关说法正确的是( )
 发布:2025/1/15 8:0:2组卷:20引用:2难度:0.8
发布:2025/1/15 8:0:2组卷:20引用:2难度:0.8 -
3.实验室中模拟用甲烷与氯气反应得到的副产品来制取盐酸,原理如图,下列说法不正确的是( )
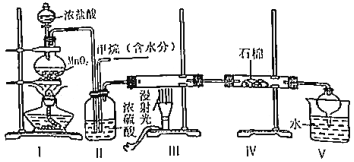 发布:2024/12/30 17:0:5组卷:61引用:1难度:0.7
发布:2024/12/30 17:0:5组卷:61引用:1难度:0.7


