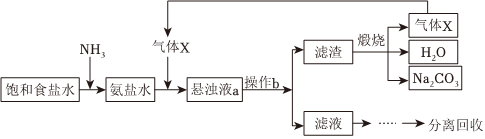
联合制碱法(又称侯氏制碱法),因其提高了食盐的转化率,减少了对环境的污染,从而赢得了国际化工界的高度评价。联合制碱法的主要过程如图1所示:
 已知:沉淀池中的反应原理如下:
已知:沉淀池中的反应原理如下:
ⅰ.NH3+CO2+H2O═NH4HCO3
ⅱ.NaCl+NH4HCO3═NaHCO3↓+NH4Cl
(1)“侯氏制碱法”中的“碱”为 Na2CO3Na2CO3(填化学式);写出煅烧炉中反应的化学方程式:2NaHCO3 △ Na2CO3+CO2↑+H2O2NaHCO3 △ Na2CO3+CO2↑+H2O。
(2)在饱和食盐水中先通入NH3,再通入CO2,这样操作的目的是 先通入氨气使溶液呈碱性,能吸收大量的二氧化碳气体,增大碳酸氢根离子的浓度,有利于析出更多的碳酸氢钠先通入氨气使溶液呈碱性,能吸收大量的二氧化碳气体,增大碳酸氢根离子的浓度,有利于析出更多的碳酸氢钠。
(3)从“母液”中可得到的副产品为 NH4ClNH4Cl,用途是 作肥料作肥料(任写一种)。
(4)“循环Ⅱ”中参与循环的物质除水外还有 CO2CO2。
(5)常温下,在10mL0.1mol•L-1Na2CO3溶液中逐滴加入0.1mol•L-1HCl溶液20mL,溶液中含碳元素的各种微粒的质量分数(纵轴)随溶液pH变化的部分情况如图2所示。回答下列问题:
①在同一溶液中,三种含碳微粒CO2-3、HCO-3、H2CO3不能不能(填“能”或“不能”)大量共存。
②将0.84gNaHCO3和1.06gNa2CO3混合并配成溶液,向溶液中滴加0.1mol•L-1稀盐酸。图像(图3)能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是 DD(填字母)。
△
△
CO
2
-
3
HCO
-
3
【考点】纯碱工业(侯氏制碱法).
【答案】Na2CO3;2NaHCO3 Na2CO3+CO2↑+H2O;先通入氨气使溶液呈碱性,能吸收大量的二氧化碳气体,增大碳酸氢根离子的浓度,有利于析出更多的碳酸氢钠;NH4Cl;作肥料;CO2;不能;D
△
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/21 3:0:1组卷:49引用:1难度:0.6
相似题
-
1.以NaCl为原料,可制取纯碱。Na2CO3可用侯氏制碱法制取,主要涉及如下反应:NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl;2NaHCO3
Na2CO3+CO2↑+H2O,下列有关实验室模拟侯氏制碱法的实验原理和装置正确的是( )△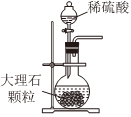
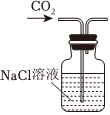
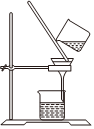
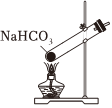
A.制取CO2 B.制取NaHCO3 C.分离NaHCO3 D.制取Na2CO3 发布:2024/12/8 18:0:1组卷:165引用:5难度:0.8 -
2.“侯氏制碱法”的主要过程如图(部分物质已略去)。
下列说法错误的是( )发布:2024/12/8 0:0:1组卷:133引用:4难度:0.7 -
3.氨碱法(索氏)和联合制碱法(侯氏)是两大重要的工业制碱法,下列表达正确的是( )
氨碱法 联合制碱法 A 原料 食盐、氨气、生石灰 食盐、氨气、二氧化碳 B 副产物 氯化钙 氯化铵 C 循环物质 氨气、二氧化碳 氯化钠 D 评价 原料易得、设备简单、能耗低 原料利用率高、废弃物少 发布:2024/12/16 6:0:1组卷:38引用:2难度:0.8


