STEM小组为测定某大理石样品中碳酸钙的质量分数,设计了两种不同的方案。(假定:样品中除碳酸钙外,其他物质均不参与反应也不溶于水)
【测量方案】
方案一:
(1)称取样品a克放入烧杯中。
(2)加入足量的稀盐酸至反应停止后,过滤、洗涤、干燥,称得滤渣为b克。
(3)求出样品中碳酸钙的质量分数为 a-ba×100%a-ba×100%(用a、b表示)。
方案二:
(1)称取样品10克放入烧杯中,将50克盐酸分5次倒入烧杯中,并不断用玻璃棒搅拌,同时称出烧杯内药品的总质量,并记录在如下表格中:
a
-
b
a
a
-
b
a
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 加入盐酸的质量/克 | 10 | 10 | 10 | 10 | 10 |
| 烧杯内药品的总质量/克 | 19.56 | 29.12 | m | 48.46 | 58.46 |
①表中m=
38.68
38.68
。②大理石样品中碳酸钙的质量分数是多少?
【评价交流】
上述两个方案,你认为哪一个方案更可行?请说明理由
方案一,由于盐酸具有挥发性,方案二会造成气体的数据偏大
方案一,由于盐酸具有挥发性,方案二会造成气体的数据偏大
。【考点】根据化学反应方程式的计算;化学实验方案的设计与评价.
【答案】×100%;38.68;方案一,由于盐酸具有挥发性,方案二会造成气体的数据偏大
a
-
b
a
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/15 1:0:2组卷:17引用:2难度:0.5
相似题
-
 1.绍兴盛产一种四角菱,称“驮背白”。其菱肉富含淀粉等多种营养物质,此外菱角的茎和根富含纤维素(C6H10O5)n,也是一种很不错的食物和药材。
1.绍兴盛产一种四角菱,称“驮背白”。其菱肉富含淀粉等多种营养物质,此外菱角的茎和根富含纤维素(C6H10O5)n,也是一种很不错的食物和药材。
(1)菱肉中的钙、磷、铁等元素是以(填“单质”或“化合物”)的形态存在;
(2)该纤维素中C、H、O元素的质量比(最简比);
(3)查阅资料获悉菱肉制成的菱粉质细爽滑,为淀粉中之佳品。求菱叶产生3.6千克淀粉[有机物(CH2O)n]的同时,光合作用产生氧气多少千克?(已知光合作用的化学方程式为:nCO2+nH2O═(CH2O)n+nO2,条件忽略)发布:2025/1/6 8:0:1组卷:4引用:1难度:0.5 -
2.小金为测定某样品中氧化铜的质量分数,称量固体样品20.0克,用如图所示的装置进行实验(杂质不参与反应且生成水完全被吸收),实验中共消耗0.6克氢气,测得B装置反应前后的质量增加了3.6克。
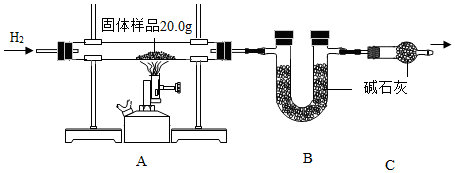
(1)C装置的作用是;
(2)计算固体样品中氧化铜的质量分数(根据化学方程式列式计算)。发布:2024/12/28 15:30:1组卷:12引用:2难度:0.5 -
3.侯德榜是我国著名的化学家,发明了侯氏制碱法,其反应原理如下:NaCl+CO2+NH3+H2O═NaHCO3+NH4Cl,请回答:
(1)反应产物中NH4C1可以用于农业生产,它属于化肥中的肥。
(2)生产16.8t碳酸氢钠,理论上需要氯化钠的质量是多少?发布:2024/12/28 15:30:1组卷:12引用:2难度:0.5


