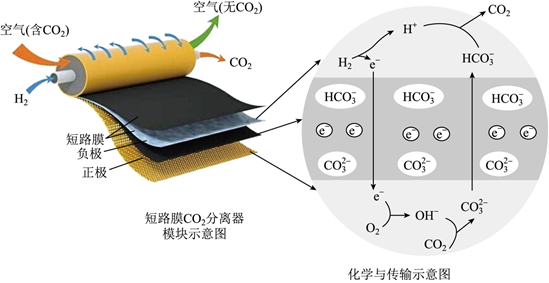
利用化学原理对废气、废水进行脱硝、脱碳处理,可实现绿色环保、废物利用,对构建生态文明有重要意义。
Ⅰ.脱硝:
(1)H2还原法消除氮氧化物
已知:N2(g)+2O2(g)═2NO2(g)ΔH=+133 kJ•mol-1
H2O(g)═H2O(l)ΔH=-44 kJ•mol-1
H2的燃烧热ΔH=-285.8 kJ•mol-1
在催化剂存在下,H2还原NO2生成水蒸气和氮气的热化学方程式为 4H2(g)+2NO2(g)=N2(g)+4H2O(g)ΔH=-1100.2kJ•mol-14H2(g)+2NO2(g)=N2(g)+4H2O(g)ΔH=-1100.2kJ•mol-1。
(2)用NH3催化还原法消除氮氧化物,发生反应:4NH3(g)+6NO(g)⇌5N2(g)+6H2O(l)ΔH<0
相同条件下,在2L恒容密闭容器中,选用不同催化剂,产生N2的量随时间变化如图所示。
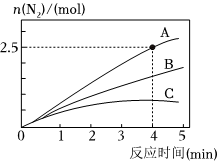
①计算0~4分钟在A催化剂作用下,反应速率v(NO)=0.375mol•L-1•min-10.375mol•L-1•min-1。
②下列说法正确的是 CDCD。
A.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
B.增大压强能使反应速率加快,是因为增加了活化分子百分数
C.单位时间内H-O键与N-H键断裂的数目相等时,说明反应已达到平衡
D.若反应在恒容绝热的密闭容器中进行,当K值不变时,说明已达到平衡
(3)利用原电池反应可实现NO2的无害化,总反应为6NO2+8NH3═7N2+12H2O,电解质溶液为NaOH溶液,工作一段时间后,该电池正极区附近溶液pH 增大增大(填“增大”“减小”或“不变”),负极的电极反应式为 2NH3-6e-+6OH-═N2+6H2O2NH3-6e-+6OH-═N2+6H2O。
Ⅱ.脱碳:
(4)用甲醇与CO反应生成醋酸可消除CO污染。常温下,将a mol•L-1醋酸与b mol•L-1 Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),忽略溶液体积变化,计算醋酸的电离常数Ka=2ba-2b×10-7L/mol2ba-2b×10-7L/mol(用含a、b的代数式表示)。
2
b
a
-
2
b
2
b
a
-
2
b
【答案】4H2(g)+2NO2(g)=N2(g)+4H2O(g)ΔH=-1100.2kJ•mol-1;0.375mol•L-1•min-1;CD;增大;2NH3-6e-+6OH-═N2+6H2O;×10-7L/mol
2
b
a
-
2
b
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/9/12 4:0:8组卷:10引用:2难度:0.6