初中实验分为定性实验和定量实验两部分,据图回答问题。
Ⅰ.定性实验
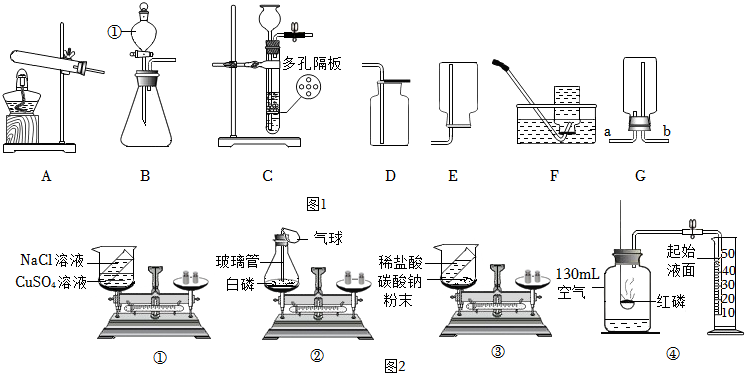
(1)图1中①仪器名称 分液漏斗分液漏斗,利用B装置制取氧气的化学反应方程式是 2H2O2 MnO2 2H2O+O2↑2H2O2 MnO2 2H2O+O2↑。
(2)实验室制取氢气的化学反应方程式为 Zn+H2SO4=ZnSO4+H2↑Zn+H2SO4=ZnSO4+H2↑;实验中小明发现反应过了半个小时依然没有停止。为了实验安全并节约药品,需要及时终止反应,此时应选择的最佳装置为 CC。
Ⅱ.定量实验
(3)小组设计实验探究质量守恒定律的装置如图2,在①至③中可选的装置是 ②②,②中气球的作用 形成密闭装置和平衡气压形成密闭装置和平衡气压。
(4)图4可用于空气中氧气含量测定,冷却室温后,量筒中液面理论上约降低到 2424mL刻度线处。(提示:量筒的起始值是50mL)
(5)某工厂化验室用15%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液40g,洗涤后的溶液呈中性,这一定量石油产品中含H2SO4的质量是多少?
M
n
O
2
M
n
O
2
【答案】分液漏斗;2H2O2 2H2O+O2↑;Zn+H2SO4=ZnSO4+H2↑;C;②;形成密闭装置和平衡气压;24
M
n
O
2
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/7/14 8:0:9组卷:27引用:1难度:0.5
相似题
-
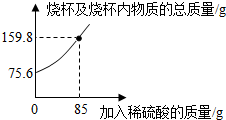 1.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为52.2g的烧杯中,然后缓慢加入一定质量的稀硫酸,当加稀硫酸质量为85g时,反应恰好完全(杂质不反应且产生的气体全部逸出),反应过程中的质量关系如图.完成下列问题:
1.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为52.2g的烧杯中,然后缓慢加入一定质量的稀硫酸,当加稀硫酸质量为85g时,反应恰好完全(杂质不反应且产生的气体全部逸出),反应过程中的质量关系如图.完成下列问题:
(1)该实验取用的样品质量为g.
(2)计算样品中铁的质量分数(写出解题过程).发布:2025/1/9 8:0:2组卷:139引用:39难度:0.1 -
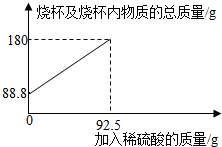 2.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为51.8克的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入92.5g稀硫酸时恰好完全反应,加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图。
2.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为51.8克的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入92.5g稀硫酸时恰好完全反应,加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图。
(1)该实验取用的样品质量为g。
(2)反应后所得溶液中的溶质的质量分数。(写出计算过程,结果保留一位小数)
(3)反应结束后,小明不慎向烧杯中多加了10g稀硫酸,若在图中补绘此过程中稀硫酸的质量与烧杯及烧杯内物质的总质量的关系图,所得线段的终点位于线段AB延长线的(填:上方、下方或线上)。发布:2025/1/9 8:0:2组卷:4引用:1难度:0.3 -
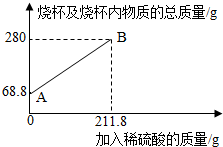 3.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为51.8克的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入211.8g稀硫酸时恰好完全反应,加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图。
3.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为51.8克的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入211.8g稀硫酸时恰好完全反应,加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图。
(1)该实验取用的样品质量为g。
(2)求样品中铁的质量分数;反应后所得溶液中的溶质的质量分数。(写出计算过程,结果保留一位小数)
(3)反应结束后,小明不慎向烧杯中多加了20g稀硫酸,若在图中补绘此过程中稀硫酸的质量与烧杯及烧杯内物质的总质量的关系图,所得线段的终点位于线段AB延长线的(填:上方、下方或线上)。发布:2025/1/9 8:0:2组卷:8引用:1难度:0.3


