某化学兴趣小组同学对氢氧化钠溶液与稀盐酸是否发生了化学反应进行如下实验探究。
【实验一】借助指示剂的颜色变化判断酸碱是否发生了反应,如图1所示。

(1)判断试管中两种物质发生反应的现象是溶液由 红红色变为 无无色,该反应的化学方程式为 NaOH+HCl=NaCl+H2ONaOH+HCl=NaCl+H2O。
【实验二】借助反应前后的温度变化来判断酸碱是否发生了反应,如图2所示,
(2)将盛有氢氧化钠固体的燃烧匙伸入稀盐酸中,观察到U形管中右侧红墨水液面上升,该现象 不能不能(填“能”或“不能”)证明氢氧化钠与稀盐酸发生了化学反应,理由是 氢氧化钠固体溶于水放热氢氧化钠固体溶于水放热。
(3)小组同学利用温度传感器测定盐酸与氢氧化钠溶液反应。用C的时间一温度曲线如图3所示。图①由曲线变化情况分析可知,稀盐酸与氢氧化钠溶液发生反应并 放热放热(填“放出”或“吸收”)热量。
【实验三】有同学提出还可利用pH的变化判断酸碱是否发生了反应,图4所示是小组同学利用pH传感器探究氢氧化钠溶液与稀盐酸反应的pH变化曲线。

(4)图4中能说明酸碱恰好完全反应的点是 BB(填“A”、“B”、“C”)。
(5)B点所示溶液中含有的阳离子为 Na+Na+(填离子符号)。
【答案】红;无;NaOH+HCl=NaCl+H2O;不能;氢氧化钠固体溶于水放热;放热;B;Na+
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/6/11 8:0:9组卷:34引用:2难度:0.5
相似题
-
1.化学兴趣小组的同学在进行酸和碱的性质探究时,进行了图一、图二、图三等三个实验:
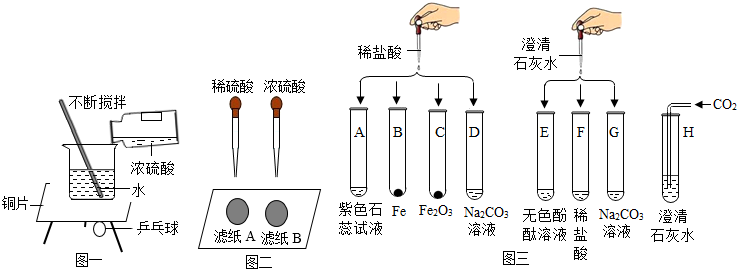
(1)【实验一】浓硫酸稀释过程中的能量变化。
图一实验中,观察到用石蜡固定在铜片下的乒乓球脱落,说明浓硫酸稀释时(填“吸热”或“放热”)
(2)【实验二】溶液浓度对硫酸化学性质的影响。
图二实验中,观察到很快变黑的是滤纸(填“A”或“B”),由此可知,硫酸溶液的浓度不同,性质不同。
(3)【实验三】探究盐酸和氢氧化钙的化学性质,取8支试管分别用A-H编号后,做如图三的实验。
①实验中观察到有气泡生成的试管是(填编号);
②试管C中反应的化学方程式为。
③实验后某试管中为红色溶液,当向其中加入过量的澄清石灰水后,溶液变为蓝色。由此推断,该试管是。(填编号)
④H试管的反应常用来检验二氧化碳,请写出反应的化学方程式。
⑤E、F、G试管实验完成后,将试管内清液都倒入同一只洁净的大烧杯中,发现有白色沉淀生成,上层清液呈无色。上层清液中溶质的成分除酚酞外一定有,可能还有。发布:2024/12/25 12:0:1组卷:95引用:5难度:0.5 -
2.某化学兴趣小组的同学利用实验室器材进行了实验探究

[实验一]如图1是实验室常用的几种实验装置,请回答下列问题:
(1)写出实验室用AE装置组合制取某种气体的化学方程式,用E装置收集该气体,气体从(填“a”或“b”)端进入。
(2)实验室制取的CO2中常含有少量杂质气体会干扰F实验的目的。为排除干扰,除去该杂质并检验是否除净,将产生的混合气体依次通过上述装置(在B至E中选择,填序号,装置不重复),再进入F装置:F装置内产生的现象为。
[实验二]探究酸碱中和反应。利用图2装置进行实验,实验开始后将注射器内的液体逐滴注入烧瓶内。
(1)实验测得烧杯中溶液的pH随时间的变化关系如图3所示,c点所示溶液加热蒸干所得固体是(填化学式)。
(2)该反应是放热反应,对应图3中点温度最高。
(3)能说明盐酸和氢氧化钠发生化学反应的依据是:
①溶液的颜色从红色变为无色;②溶液的pH。
[实验三]探究NaOH和CO2的反应。
(1)从压强变化的角度探究。
①利用图4装置进行实验,先挤压胶头滴管,再打开止水夹,观察到烧瓶内形成红色“喷泉”,原因是烧瓶内压强(填“大于”或“小于”)外界大气压;
②利用图5装置进行实验,分别将等体积的NaOH溶液和水同时注入盛有等体积CO2的玻璃容器中。证明CO2与NaOH溶液发生反应的实验现象是。
(2)利用“数字化实验”探究。利用图6装置进行实验,实验过程中装置内压强变化如图7所示,a点时推入NaOH溶液,b点时推入稀盐酸。
①ab段对应反应的化学方程式;
②bc段压强不变的原因是;
③证明CO2与NaOH溶液发生反应的实验现象是。发布:2024/12/25 16:30:1组卷:153引用:2难度:0.3 -
3.在实验课上,同学们将CO2通入到Ca(OH)2溶液中观察到有白色沉淀生成,而将CO2通入到NaOH溶液中无明显现象。
【提出问题】CO2与NaOH溶液是否发生了化学反应?
【提出猜想】CO2与NaOH溶液发生了化学反应
【实验探究】小明设计出了下列4种实验装置,其共同原理是二氧化碳和氢氧化钠溶液反应,使容器内压强降低。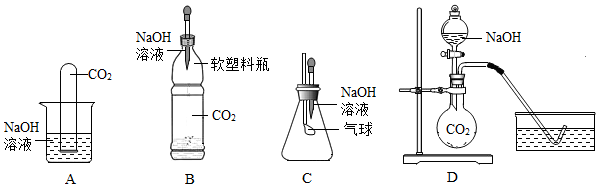
(1)实验现象为:A中试管内液面上升,B中,C中,D中水槽中的水部分进入烧瓶。
(2)小宁对小明的方案提出了质疑,他认为小明的实验不严谨,其理由是要得到科学严谨的结论,利用方案A,补做的对比实验是。
(3)小丽的改进方案是利用反应后的溶液来验证猜想,请完成实验报告。
【得出结论】CO2与NaOH溶液发生了化学反应,请写出CO2与NaOH反应的化学方程式:实验操作 实验现象 实验结论 向实验后的溶液
中加入稀盐酸猜想正确 。发布:2024/12/25 11:0:2组卷:73引用:3难度:0.1


