当前位置:
知识点挑题
请展开查看知识点列表
>
<
更多>>
|
原创
 更新中
更新中
|
知识梳理
总结方法
剖析考点
配加典例
浏览次数:2331
更新:2025年04月27日
|
 已完结
已完结
|
真题汇编
专项突破
夯实基础
稳步提升
浏览次数:82
更新:2025年04月27日
|
 2731.人类在探索物质世界和微观世界的历史长河中,充满了智慧。请你回答相关问题。
2731.人类在探索物质世界和微观世界的历史长河中,充满了智慧。请你回答相关问题。
(1)下面的科学家中最早发现电子的是(填字母)。
A.道尔顿
B.汤姆森
C.卢瑟福
D.门捷列夫
(2)“α粒子轰击金箔实验”为建立现代原子理论打下了基础。他们用一束质量远大于电子的高速运动的α粒子轰击金箔,发现:“大多数α粒子能穿过金箔,一小部分发生偏转,极少数被反弹回来。”
①根据实验现象中α粒子“大多数”与“极少数”的对比分析,你能想象出关于Au原子结构的结论是。
②该实验揭示了原子是由和构成的。
(3)原子是一种看不见、摸不着的微粒,为了帮助人们理解原子的结构,科学家都运用了来表达他们的理论成果。
(4)碳-12、碳-13、碳-14都是碳元素的原子,它们的主要差别在于。
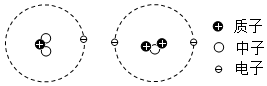
(5)人们很早就意识到物质都是由几种亘古不变的基本成分“元素”组成的。如图是两个微粒的结构模型示意图,这两个微粒是否属于同种元素?你的观点及依据是。发布:2024/12/12 8:0:1组卷:96引用:3难度:0.62732.LiFePO4电池具有高稳定,环保等优点,已知其中Li和P的化合价分别为+1价和+5价,则Fe的化合价为( )
发布:2024/12/12 8:0:1组卷:1引用:1难度:0.72733.用化学用语填空:
(1)氦气:;
(2)氯化铁;
(3)硫酸根离子:;
(4)2个镁离子:;
(5)P2O5中P的化合价:.
(6)“3O2”数字的化学意义,3表示,表示.发布:2024/12/12 8:0:1组卷:3引用:1难度:0.52734.化学与社会发展有着密切的联系.请回答下列有关问题:
(1)发展氢能源有着广阔的前景,有研究人员提出了“利用太阳能,以水为原料,大量生产氢气,并用作各种机械的动力燃料”这一设想.你认为这一设想能否实现?.能若认为能写出有关的两个化学方程式、.
用氢气作为燃料与现在广泛使用的化石燃料相比有什么优点?(要求答出两点)
①;②.
(2)为了降低汽车尾气对空气的污染,可用纳米级的某种氧化物作催化剂,使尾气中的CO与氮氧化物(NO)反应,转化为空气中含有的两种气体(其中一种为单质),该反应的化学方程式为,其中NO发生了(填“氧化”或“还原”)反应.
(3)超临界CO2流体是一种与水相似,能阻燃、溶解能力强的溶剂,被誉为“绿色环保溶剂”.它作为“绿色环保溶剂”的原因之一是能代替许多有害、有毒、易燃的有机溶剂;之二是.
(4)Na2FPO3是某种含氟牙膏成分之一,已知F为-1价,则P的化合价为.发布:2024/12/12 8:0:1组卷:10引用:1难度:0.3 2735.硫酸铜是生产、生活中常见的物质,下面是某学习小组展开的探究实录:
2735.硫酸铜是生产、生活中常见的物质,下面是某学习小组展开的探究实录:
Ⅰ、硫酸铜的制备
(1)某学习小组同学利用铜屑、稀硫酸为原料制备硫酸铜.其原理是在高温条件下将铜粉反复灼烧,使铜充分氧化成氧化铜,再将氧化铜与稀硫酸反应制备硫酸铜,请写出相应的化学方程式、;
(2)通过查阅资料,同学们找到了一种工业制备硫酸铜晶体(CuSO4•xH2O)的流程,具体如下:将铜丝放到稀硫酸中,控温在50℃.加入10%的H2O2,反应0.5h后,升温到60℃,持续反应1h后,过滤、蒸发、降温结晶等,用少量95%的酒精淋洗后晾干,得CuSO4•5H2O.
①写出该工艺流程生成CuSO4的化学方程式;
②在上述生产过程中,控制温度在50℃和60℃加热的原因为,
③上述生产流程的优点有(写出一种即可);
④在过滤时,采用了右图所示的装置,你认为这样做的优点是;
Ⅱ、硫酸铜的应用及相关实验
(1)波尔多液是用硫酸铜和石灰乳配成的一种天蓝色、粘稠的悬浊液,其有效成分是Cu4(OH)6SO4,其中铜元素的化合价为,该化学式可以写成盐和碱的形式,其杀菌机理可看作是Cu2+使病原菌失去活性,这说明病原菌的主体是(填一种有机物名称).
(2)为验证Al的化学性质比铜活泼,小怡做了以下实验,现象如下表:
认真分析上表,回答下列问题:Al片(未打磨) Al片(打磨) CuSO4溶液
(5%,5mL)无变化,数小时后铝片上附有极少气泡,几乎无红色物质 极少气泡,附着极少红色物质,持续较长时间 CuSO4溶液
(10%,5mL)无变化,数小时后铝片附有稍多气泡,仅有极少红色斑点 稍多气泡,附着极少(多于5%)红色物质,持续较长时间 CuCl2溶液
(5%,5mL)多量气泡,迅速出现红色物质,很快溶液变成无色,且温度升高 更多量气泡,迅速出现红色物质,很快溶液变成无色,且温度升高
①铝和铜盐溶液反应速率与、和有关,同时说明铜盐溶液中的Cl-能(填“加快”或“抑制”)反应速率,若实验室没有CuCl2溶液,则可以在CuSO4溶液中加入少许(填物质名称),以使实验现象更为明显;
②该反应过程要(填“吸热”或“放热”).经检验,产生的气体是一种能燃烧的单质,该气体是(填化学式);
Ⅲ、硫酸铜晶体(CuSO4•xH2O)中结晶水(xH2O)含量的测定
在老师的指导下,学习小组取12.5g硫酸铜晶体(CuSO4•xH2O)进行热分解,获得相关数据,并绘制成固体质量-温度的关系如下图.
(1)在加热过程中,随着水分的蒸发,固体颜色将由蓝色逐渐变为色,最终变为黑色;
(2)写出固体质量由10.7g变为8.9g时的化学方程式;
(3)650℃以上时,硫酸铜固体就会发生分解,生成黑色金属氧化物、二氧化硫及氧气,此反应的化学方程式为;
(4)根据图中数据,计算CuSO4•xH2O中的CuSO4的质量分数.(要求:根据x的值进行计算,CuSO4的相对分子质量:160,H2O的相对分子质量:18)发布:2024/12/12 8:0:1组卷:69引用:1难度:0.12736.废弃电路板中含有大量可利用的塑料、玻璃、金属等物质,利用超临界水技术处理废弃电路板,能得到由CuO和Cu2O组成的固体残渣,将残渣进行进一步处理可得硫酸铜晶体等物质。处理流程如图所示。
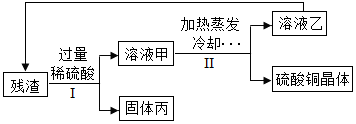
已知:Cu2O+H2SO4═CuSO4+Cu+H2O。
(1)固体丙是。
(2)溶液甲中的溶质有。
(3)下列说法不正确的是(填字母序号)。
A.Ⅰ中含过滤操作,Ⅱ中不含过滤操作
B.溶液甲和溶液乙中均含铜元素
C.残渣的处理流程中,理论上有二分之一的铜元素转化成硫酸铜晶体发布:2024/12/12 8:0:1组卷:33引用:1难度:0.52737.硫酸铜晶体常用作农业和渔业的杀虫剂、杀菌剂。以下是由废铜料(含铁)生产硫酸铜晶体的流程。

(1)B的化学式为,操作a的名称是。
(2)反应②、③的基本类型分别为、;反应①、③的化学方程式分别为①;。发布:2024/12/12 8:0:1组卷:11引用:1难度:0.52738.磷酸亚铁锂(LiFePOx)新型锂离子动力电池以其独特的优势成为绿色能源的新宠,已知Li的化合价为+1、P的化合价+5,则x的值为( )
发布:2024/12/12 8:0:1组卷:124引用:3难度:0.52739.今年四月因遭受“倒春寒”导致部分地区小麦生长发育不良,出现了叶片干枯等症状,对此专家提出使用KH2PO4溶液喷洒小麦叶片.下列说法中正确的是( )
发布:2024/12/12 8:0:1组卷:7引用:1难度:0.72740.现在大型电动车辆公交车、电动汽车、景点游览车及混合动力车等广泛应用磷酸亚铁锂电池(LiFePO4),它具有“高效率输出、高温时性能良好、极好的循环寿命、可快速充电、低成本、无记忆效应、体积小、重量轻、环保”等优点.回答问题:
(1)密度最小的金属为.
(2)已知磷酸亚铁锂中,Li为+1价,Fe为+2价,则P的化合价为.
(3)磷酸亚铁锂中铁、氧元素的质量比为.
(4)磷酸亚铁锂的相对分子质量为.
(5)磷酸亚铁锂中磷元素的质量分数为(精确到0.1%)发布:2024/12/12 8:0:1组卷:11引用:1难度:0.3



