当前位置:
知识点挑题
请展开查看知识点列表
>
<
更多>>
|
原创
 更新中
更新中
|
暑假预习
夯实基础
活学活用
人教版(2024)
沪教版(2024)
浏览次数:253
更新:2025年06月19日
|
 已完结
已完结
|
中考模拟
分类汇编
专项突破
浏览次数:3205
更新:2025年06月17日
|
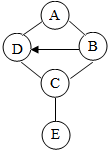 661.图中A、B、C、D、E是初中化学常见的五种不同类别的物质。E是导致温室效应的一种气体,图中“-”表示相连物质能发生化学反应,“→”表示两种物质间的转化关系(部分反应物、生成物及反应条件省略)。
661.图中A、B、C、D、E是初中化学常见的五种不同类别的物质。E是导致温室效应的一种气体,图中“-”表示相连物质能发生化学反应,“→”表示两种物质间的转化关系(部分反应物、生成物及反应条件省略)。
(1)写出物质E的一种用途;
(2)物质C与E反应的化学方程式是;
(3)写出图中一个属于中和反应的化学方程式。
(4)A与B反应的微观实质是。发布:2024/12/25 15:30:1组卷:254引用:6难度:0.1662.模型认知是化学研究的重要科学方法。如图是工业制取硝酸第一步反应的微观示意图。下列说法不正确的是( )
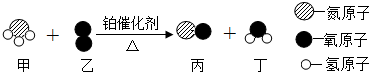 发布:2024/12/25 15:30:1组卷:254引用:17难度:0.6
发布:2024/12/25 15:30:1组卷:254引用:17难度:0.6663.大量硝酸钾固体中混有少量的氯化钠,常采用降温结晶的方式除杂,氯化钠不析出的原因是( )
发布:2024/12/25 15:30:1组卷:466引用:2难度:0.7664.推理是化学学习中常用的思维方法.下列推理正确的是( )
发布:2024/12/25 15:30:1组卷:725引用:59难度:0.9665.我市一家企业生产的“土豆农膜”是一种新型环保农膜,在塑料中添加土豆淀粉,可被细菌和微生物释放的酶分解,使塑料呈多孔状,强度下降。下列有关说法错误的是( )
发布:2024/12/25 15:30:1组卷:355引用:13难度:0.9666.碳酸氢钠是一种应用广泛的盐,化学小组对其进行了探究。
(1)NaHCO3可称为钠盐或碳酸氢盐,它是由Na+和(填离子符号)构成,医疗上能用于治疗胃酸(含有盐酸)过多症,反应的化学方程式为。
【提出问题】实验室中如何制取少量NaHCO3?
【查阅资料】
材料一:侯氏制碱的原理:NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl;2NaHCO3Na2CO3+CO2↑+H2O。△
材料二:研究发现,NaHCO3溶于水时吸收热量,Na2CO3溶于水时放出热量。
【实验制备】根据侯氏制碱原理设计如图1所示装置制取NaHCO3。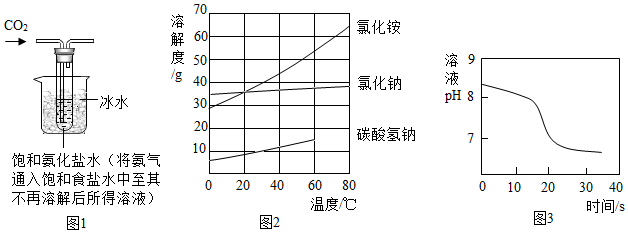
反应结束后,将试管中的混合物过滤洗涤,低温烘干得白色固体。
(2)烧杯中冰水的作用是。
(3)能进一步确认该白色固体是NaHCO3的实验方案是(须用到的仪器和药品:试管、温度计、水)。
(4)如图2中碳酸氢钠的溶解度在60℃后无数据的原因可能是。
【性质探究】
常温下,取一定量的NaHCO3溶液于烧杯中,插入pH传感器,向烧杯中持续滴加CaCl2溶液,有白色沉淀生成,当溶液的pH变为6.68时开始有无色气体产生。反应过程中溶液的pH随时间变化如图3所示。
【查阅资料】
材料三NaHCO3溶于水后,少量的能同时发生如下变化:HCO-3
变化①:+H2O→H2CO3+OH-;HCO-3
变化②:→HCO-3+H+。CO2-3
材料四:溶液的酸碱性与溶液中H+和OH-数目的相对大小有关。常温下,当单位体积溶液中OH-的数目大于H+的数目时溶液的pH>7,反之pH<7;单位体积溶液中所含的H+数目越大,溶液的pH越小。
【交流反思】
(5)NaHCO3溶液显(填“酸”“碱”或“中”)性,结合材料三、四从微观角度说明原因:。
(6)根据本实验,下列说法错误的是(填字母)。
a.pH<6.68时生成的无色气体为CO2
b.从0~30s,单位体积溶液中H+数目不断增大
c.不能用CaCl2溶液鉴别Na2CO3和NaHCO3溶液发布:2024/12/25 15:30:1组卷:591引用:4难度:0.5667.请完成以下实验报告的填写.
实验名称:酸和碱的中和反应
实验目的:验证盐酸和氢氧化钠能否发生反应.
供选择的仪器和药品:试管、胶头滴管、烧杯、酚酞溶液、稀盐酸、氢氧化钠稀溶液.实验步骤 实验现象 实验结论、解释 (1)在 中加入约1mL氢氧化钠稀溶液,用胶头滴管滴入几滴酚酞溶液.溶液显 色碱能使酚酞溶液变色 (2)然后, ,直至溶液恰好变无色为止.溶液颜色最后褪去 两者能发生反应,反应的化学方程式是 .发布:2024/12/25 15:30:1组卷:526引用:38难度:0.5668.下表中列出了几种物质的熔点,据此判断下列说法正确的是( )
物质名称 汞 金 铜 铁 钨 氧 熔点/℃ -38.8 1064 1083 1535 3410 -218 发布:2024/12/25 15:30:1组卷:542引用:10难度:0.9669.下列从原料及有关试剂分别制取相应的最终产物的设计中,理论上正确、操作上可行、经济上合理的是( )
发布:2024/12/25 15:30:1组卷:665引用:25难度:0.7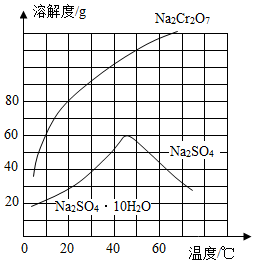 670.如图为两物质的溶解度曲线。请回答:
670.如图为两物质的溶解度曲线。请回答:
(1)50℃时Na2Cr2O7的溶解度为g,60℃时溶解度:Na2Cr2O7Na2SO4 (填“<”、“=”、“>”)。
(2)在50℃时,把210g Na2Cr2O7饱和溶液降温到10℃,析出Na2Cr2O7g(假设不含结晶水)。发布:2024/12/25 15:30:1组卷:354引用:12难度:0.7



