当前位置:
知识点挑题
请展开查看知识点列表
>
<
更多>>
 已完结
已完结
|
期末复习
典型试卷
考前必刷
浏览次数:2088
更新:2025年06月03日
|
 已完结
已完结
|
热点预测
高考复习
难题抢练
浏览次数:1552
更新:2025年05月26日
|
 1051.铜锌原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( )发布:2024/12/30 14:30:1组卷:14引用:3难度:0.7
1051.铜锌原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( )发布:2024/12/30 14:30:1组卷:14引用:3难度:0.71052.下列说法正确的是( )
发布:2024/12/30 14:30:1组卷:26引用:2难度:0.71053.A元素原子的第2层比B元素原子的第2层少3个电子,B元素的原子核外电子总数比A元素原子的核外电子总数多5个,则A与B可形成的化合物类型为( )
发布:2024/12/30 14:30:1组卷:12引用:2难度:0.91054.下列物质的电子式书写正确的是( )
发布:2024/12/30 14:30:1组卷:25引用:2难度:0.61055.根据下列两个反应判断:2Cu+O2=2CuO,2Cu+S=Cu2S,下列叙述中错误的是( )
发布:2024/12/30 14:30:1组卷:16引用:2难度:0.91056.最近科学家发现了氧元素的一种新的粒子04.对于这种新粒子,下列说法不正确的是( )
发布:2024/12/30 14:30:1组卷:13引用:2难度:0.9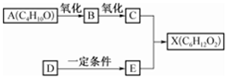 1057.如图中X是无支链的、具有果香味的合成香料,可用于调配多种果香型香精.已知D在标准状况下的密度为1.25g•L-1,其产量可以用来衡量一个国家石油化工发展水平.E是生活中常见的一种有机物.各物质间转化关系如图:
1057.如图中X是无支链的、具有果香味的合成香料,可用于调配多种果香型香精.已知D在标准状况下的密度为1.25g•L-1,其产量可以用来衡量一个国家石油化工发展水平.E是生活中常见的一种有机物.各物质间转化关系如图:
请回答下列问题:
(1)A的名称是,B中所含的官能团是.
(2)C+E→X的化学反应类型是反应.
(3)写出任意两种与A 具有相同官能团的A 的同分异构体的结构简式(不包括A ):
(4)X与氢氧化钠溶液反应的化学方程式是.
(5)以D为原料生产一种常见塑料的化学方程式是.发布:2024/12/30 14:30:1组卷:12引用:3难度:0.31058.检验SO2中是否混有CO2气体,可采用的方法是( )
发布:2024/12/30 14:30:1组卷:14引用:4难度:0.91059.下列对实验内容的解释正确的是( )
编号 实验内容 解释 A 将少量Fe(NO3)2试样加水溶解,滴加稀F2SO4酸化,再滴加KSCN溶液,溶液变成红色 Fe(NO3)2试样已变质 B 向饱和Na2CO3溶液中通入CO2,溶液变浑浊 析出了NaHCO3晶体 C 取1mL蔗糖溶液,加入3滴稀H2SO4,水浴加热5min,冷却后加入少量新制Cu(OH)2悬浊液,加热,未产生砖红色沉淀 蔗糖水解产物中不含有葡萄糖 D 向NaHCO3溶液中滴加NaAlO2溶液,有白色沉淀和气体产生 HCO3-和AlO2-发生了双水解 发布:2024/12/30 14:30:1组卷:29引用:2难度:0.5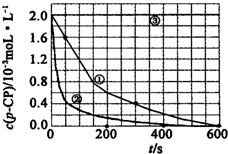 1060.(一)Fenton法常用于处理含有难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物.现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响.实验中控制p-CP的初始浓度相同,恒定实验温度在298K或313K下设计如下对比实验(其余实验条件见下表):
1060.(一)Fenton法常用于处理含有难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物.现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响.实验中控制p-CP的初始浓度相同,恒定实验温度在298K或313K下设计如下对比实验(其余实验条件见下表):
(1)编号③的实验目的是实验序号 实验目的 T/K pH c/10-3mol•L-1 H2O2 Fe2+ ① 为以下实验作参照物 298 3 6.0 0.30 ② 探究温度对降解反应速率的影响 313 3 6.0 0.30 ③ 298 10 6.0 0.30 .
(2)实验测得不同实验编号中p-CP的浓度随时间变化的关系如图所示.请根据实验①曲线,计算降解反应在50-300s内的平均反应速率v(p-CP)=.
(3)实验①②表明,温度与该降解反应速率的关系是.
(二)已知Fe3+和I-在水溶液中的反应为2I-+2Fe3+=2Fe2++I2.正向反应速率和I-、Fe3+的浓度关系为v=kcm(I-)cn(Fe3+)(k为常数)
(4)请分析下表提供的数据回答以下问题:
①在v=kcm(I-)cn(Fe3+)中,m、n的值为c(I-)/(mol•L-1) c(Fe3+)/(mol•L-1) v/(mol•L-1•s-1) (1) 0.20 0.80 0.032k (2) 0.60 0.40 0.144k (3) 0.80 0.20 0.128k .(选填A、B、C、D)
A.m=1,n=1 B.m=1,n=2 C.m=2,n=1 D.m=2,n=2
②I-浓度对反应速率的影响Fe3+浓度对反应速率的影响(填“<”、“>”或“=”).
(三)一定温度下,反应FeO(s)+CO(g)⇌Fe(s)+CO2(g)的化学平衡常数为3.0,该温度下将2mol FeO、4mol CO、5mol Fe、6mol CO2加入容积为2L的密闭容器中反应.请通过计算回答:
(5)v(正)v(逆)(填“>”、“<”或“=”);若将5mol FeO、4mol CO加入同样的容器中,在相同温度下达到平衡,则CO的平衡转化率为.发布:2024/12/30 14:30:1组卷:20引用:2难度:0.5



