当前位置:
知识点挑题
请展开查看知识点列表
>
<
更多>>
 已完结
已完结
|
期末复习
典型试卷
考前必刷
浏览次数:1406
更新:2025年06月03日
|
 已完结
已完结
|
热点预测
高考复习
难题抢练
浏览次数:1351
更新:2025年05月26日
|
2851.下列说法正确的是( )
发布:2024/12/21 8:0:2组卷:14引用:1难度:0.9 2852.X、Y、Z、W四种短周期元素在周期表中的位置关系如图:
2852.X、Y、Z、W四种短周期元素在周期表中的位置关系如图:
I.若Y元素原子的最外层电子数是电子层数的3倍
(1)W的原子结构示意图为。
(2)Z在周期表中的位置。
(3)一定条件下,X的最低价氢化物与X的某种氧化物按2:3物质的量比混合恰好反应生成X 单质和水,该氧化物的化学式为。
(4)写出铜片置于Z的最高价氧化物水化物稀溶液,没有明显变化。加热,依然如故。再通入空气,溶液就逐渐变蓝,使溶液变蓝的反应的离子方程式:。
Ⅱ.若Y和Z的核外电子数之和为20。
(5)相对分子质量为16的Y的氢化物电子式为。
(6)写出单质Y和浓硝酸反应的化学方程式:。
(7)写出工业制备Z的过程中发生的第一个反应的化学方程式。发布:2024/12/21 8:0:2组卷:4引用:1难度:0.52853.某种酒精与水的混合物中,酒精分子与水分子的个数比为5:6,则该混合物中酒精(化学式C2H6O)的质量分数为( )
发布:2024/12/21 8:0:2组卷:33引用:3难度:0.72854.下列说法正确的是( )
发布:2024/12/21 8:0:2组卷:5引用:1难度:0.82855.工业上可以用植物秸秆等富含纤维素的废弃物为原料生产葡萄糖,然后再生产乙醇,葡萄糖和乙醇都具有很多重要用途.请应用有机化学知识解答下列问题.
(1)写出纤维素转化为葡萄糖的化学方程式:.
(2)将葡萄糖溶液与新制氢氧化铜悬浊液混合并加热至沸腾,产生的现象是.
(3)在铜或银催化和加热条件下,乙醇能被氧气氧化为有机化合物X,写出该反应的化学方程式:;X能再被氧气氧化生成一种有酸味的液态有机化合物Y,Y所含官能团的结构简式和名称分别是.
(4)在浓硫酸存在和加热条件下,乙醇与Y发生反应生成一种液态有机化合物W,该反应的化学方程式是,反应类型是.
(5)鉴别液态有机化合物Y与W,可以采用“不用化学试剂法”,也可以采用“只用一种化学试剂法”.采用不用化学试剂法的根据是;采用只用一种化学试剂法时,在家庭厨房里可选用的化学试剂的名称是.
(6)实验室中分离有机化合物Y和水的混合物的方法是;分离有机化合物W和水的混合物的方法是.
(7)有机化合物Y和淀粉、大豆油和食盐都是人们的日常生活中必不可少的物质,其中属于高分子化合物的是,属于无机物的是.
(8)乙醇可发生化学反应生成乙烯,乙烯又可发生化学反应生成聚乙烯,乙烯生成聚乙烯的化学反应类型是.发布:2024/12/21 8:0:2组卷:28引用:0难度:0.92856.下列说法不合理的是( )
发布:2024/12/21 8:0:2组卷:2引用:1难度:0.9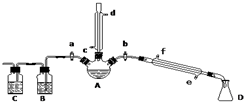 2857.某兴趣小组在实验室用加热乙醇、浓H2SO4、溴化钠和少量水的混合物来制备溴乙烷,并检验反应的部分副产物.设计了如图装置,其中夹持仪器、加热仪器及冷却水管没有画出.请根据实验步骤回答:
2857.某兴趣小组在实验室用加热乙醇、浓H2SO4、溴化钠和少量水的混合物来制备溴乙烷,并检验反应的部分副产物.设计了如图装置,其中夹持仪器、加热仪器及冷却水管没有画出.请根据实验步骤回答:
(1)仪器A的名称是,仪器A正上方冷凝管冷凝水从口进入,仪器A右方冷凝管冷凝水从口进入;
(2)制备操作中,加入的少量的水,其目的是(填字母);
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(3)加热片刻后,A中的混合物出现橙红色,该橙红色物质可能是;
(4)理论上上述反应的副产物还可能有:乙醚(CH3CH2-O-CH2CH3)、乙烯、溴化氢等
①检验副产物中是否含有溴化氢:熄灭酒精灯,在竖直冷凝管上方塞上塞子、打开a,利用余热继续反应直至冷却,通过B、C装置检验.B、C中应盛放的试剂分别是、;
②检验副产物中是否含有乙醚:通过红外光谱仪鉴定所得产物中含有“-CH2CH3”基团,来确定副产物中存在乙醚.你认为对该同学的观点;(填“正确”或“不正确”),原因是.发布:2024/12/21 8:0:2组卷:93引用:1难度:0.12858.X、Y元素最外层电子数相同,核内质子数均小于20,X元素能显正价,也能显负价,且正、负价绝对值相等,它的氢化物中氢元素的质量分数为
,Y能生成难溶于水的氧化物,其中X元素与氧元素的质量比为7:8.通过计算确定X、Y各是什么元素.14发布:2024/12/21 8:0:2组卷:6引用:0难度:0.92859.根据要求写出反应的方程式:
(1)Na投到冷水中的离子方程式;
(2)Al和氢氧化钠溶液反应的离子方程式;
(3)Cu和稀硝酸反应的离子方程式;
(4)氢氧化钙与氯化铵反应的化学方程式。发布:2024/12/21 8:0:2组卷:76引用:1难度:0.62860.化学是一门以实验为基础的自然科学,化学实验在化学学习中具有重要作用。
(1)下列关于实验的叙述中正确的有(填字母)。
A.不慎碰翻燃着的酒精灯使酒精在桌面上燃烧起来,应立即用湿抹布灭火
B.不慎将酸沾到皮肤或衣物上,应立即用浓NaOH溶液清洗
C.先在天平两个托盘上各放一张相同质量的纸,再把氢氧化钠固体放在纸上称
D.把试剂瓶中的Na2CO3溶液倒入试管中,发现取量过多,为了不浪费,又把多余的试剂倒入原试剂瓶中
E.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
F.使用分液漏斗前要检查其是否漏水
G.用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液中的水全部加热蒸干
(2)可用于分离或提纯物质的方法有:a.过滤;b.结晶;c.蒸馏;d.加热;e.分液。
请将相应分离提纯物质方法的序号填入空白处:
①除去澄清石灰水中悬浮的CaCO3颗粒:。
②除去CaO中混有的CaCO3:。
③分离酒精和水的混合物:。
④分离水和CCl4的混合物:。
(3)实验室配制100mL 0.5mol/L的盐酸。
①下列关于容量瓶的使用方法中,正确的是(填下列选项的编号字母)。
a.使用前应检查是否漏液
b.使用前必须烘干
c.不能用作物质反应或溶解的容器
d.热溶液可直接转移到其中
②配制该溶液需用10mol/L的浓盐酸mL。
③下列操作会使配制的溶液浓度偏高的是(填下列选项的编号字母)。
A.没有将洗涤液转移到容量瓶
B.转移过程中有少量溶液溅出
C.摇匀后,液面下降,补充水
D.定容时俯视刻度线。发布:2024/12/21 8:0:2组卷:10引用:1难度:0.5



