当前位置:
知识点挑题
请展开查看知识点列表
>
<
更多>>
 已完结
已完结
|
期末复习
典型试卷
考前必刷
浏览次数:1705
更新:2025年06月03日
|
 已完结
已完结
|
热点预测
高考复习
难题抢练
浏览次数:1443
更新:2025年05月26日
|
431.氨分子的空间结构是三角锥形,而甲烷分子的空间结构是正四面体形,这是因为( )
发布:2024/12/30 18:30:1组卷:6引用:3难度:0.6432.砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等,氮、磷、砷位于同一主族,回答下列问题:
(1)写出基态As原子的核外电子排布式。
(2)根据元素周期律,原子半径GaAs,第一电离能GaAs.(填“大于”或“小于”)
(3)氮原子的L层中有对成对电子,NH4+的立体构型是,其中心原子的杂化方式为;PCl3属于含有键的分子(填“极性”或“非极性”)。发布:2024/12/30 18:30:1组卷:6引用:2难度:0.5433.白磷燃烧的能量变化如图甲所示,白磷及产物的结构如图乙所示,下列说法不正确的是( )
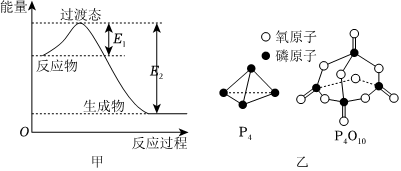 发布:2024/12/30 18:30:1组卷:14引用:4难度:0.6
发布:2024/12/30 18:30:1组卷:14引用:4难度:0.6434.处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
形象化描述.在基态14C原子中,核外存在对自旋方向相反的电子.O、Na、P、Cl四种元素中电负性最大的是(填元素符号),其中磷原子的核外电子排布式为.发布:2024/12/30 18:30:1组卷:11引用:2难度:0.5435.下列模型分别表示C2H2、S8、SF6的结构,下列说法不正确的是( )
 发布:2024/12/30 18:30:1组卷:7引用:2难度:0.5
发布:2024/12/30 18:30:1组卷:7引用:2难度:0.5436.下列有关共价键的形成的说法错误的是( )
发布:2024/12/30 18:30:1组卷:8引用:2难度:0.8437.已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
发布:2024/12/30 18:30:1组卷:7引用:3难度:0.6438.试回答下列问题:
(1)碳酸亚乙烯酯是锂离子电池低温电解液的重要添加剂,其结构为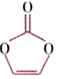 。该分子中含
。该分子中含
个σ键,已知键能数据如表所示:
则该物质与H发生加成反应时,最易断裂的化学键为化学键 C-O C-C C=C C=O 键能/(kJ•mol-1) 358 347 614 745 (填字母,下同);在碱性条件下发生取代反应(即水解反应时),最易断裂的化学键为。
a.C-O
b.C-C
c.C=C
d.C=O
(2)由短周期元素组成的含有14个电子的四核化合物,其结构式为;分子内所含σ键的数目是,π键的数目是,σ键的强度比π键的强度,原因是。
(3)X、Y、Z是元素周期表中的短周期元素,其中X、Y同周期,Y Z同主族,Y原子最外层p轨道上的电子数等于前一电子层电子总数,X原子最外层的p能级中只有一个轨道填充了2个电子,而且这三种元素可以形成化合物YX2、ZX2。根据上述信息回答下列问题:
①写出下列元素符号:X,Y,Z。
②YX2分子中含个σ键,含个π键。发布:2024/12/30 18:30:1组卷:13引用:2难度:0.8439.金属及其化合物在生产生活等各个领域有着广泛的应用。
(1)钛具有良好的金属性能。钛基态原子中电子占据能级个数为。与钛同周期的元素中,基态原子的未成对电子数与钛相同的还有种。钛比钢轻、比铝硬,是一种新兴的结构材料,钛硬度比铝大的可能原因是。
(2)有一种氮化钛晶体的晶胞与NaCl晶胞相似,该晶胞中N、Ti之间的最近距离为a×10-10cm,则该氮化钛的密度为g•cm-3(NA为阿伏加德罗常数的值,只列计算式)。
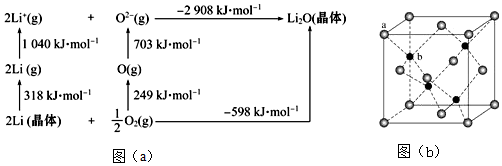
(3)Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。Li2O是离子晶体,其晶格能可通过图(a)的Bom-Haber循环计算得到。
Li原子的第一电离能为kJ•mol-1,O═O键键能为kJ•mol-1,Li2O晶格能为kJ•mol-1。
(4)Zn可形成多种化合物,其中立方ZnS晶胞结构如图(b),其阴离子(S2-)按面心立方密堆积排布,立方ZnS的配位数与NaCl不同,这是由因素决定的。发布:2024/12/30 18:30:1组卷:7引用:2难度:0.7440.下列有关叙述错误的是( )
发布:2024/12/30 18:30:1组卷:11引用:4难度:0.8



