当前位置:
知识点挑题
请展开查看知识点列表
>
<
更多>>
 已完结
已完结
|
期末复习
典型试卷
考前必刷
浏览次数:2019
更新:2025年06月03日
|
 已完结
已完结
|
热点预测
高考复习
难题抢练
浏览次数:1514
更新:2025年05月26日
|
841.元素的第一电离能(设其为I1)的周期性变化如图所示。试根据元素在元素周期表中的位置,分析图中曲线的变化特点,并回答下列问题。
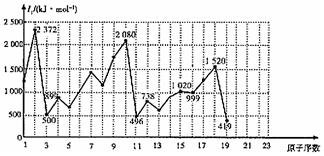
(1)同主族内不同元素的I1值变化特点是。
(2)同周期内,随原子序数增大,I1值增大。但个别元素的I1值出现反常现象。试推测下列关系式中正确的是。(填编号)
①I1(砷)>I1(硒)
②I1(砷)<I1(硒)
③I1(溴)>I1(硒)
④I1(溴)<I1(硒)
(3)推测气态基态钙原子失去最外层一个电子所需能量的范围:<I1<。
(4)10号元素I1值较大的原因是。发布:2024/12/30 16:0:2组卷:14引用:3难度:0.6842.按要求填空:
(1)基态B原子的电子排布式为。
(2)Se原子序数为,其核外M层电子的排布式为。
(3)Li3N晶体中氮以N3-存在,基态N3-的电子排布式为。
(4)写出基态镓(Ga)原子的电子排布式:。
(5)基态钒(V)原子价层电子的电子排布图(轨道表达式)为。
(6)基态Zn原子核外电子排布式为。发布:2024/12/30 16:0:2组卷:24引用:3难度:0.8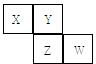 843.X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示,Y是地壳中含量最多的元素,下列说法中正确的是( )发布:2024/12/30 16:0:2组卷:19引用:2难度:0.7
843.X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示,Y是地壳中含量最多的元素,下列说法中正确的是( )发布:2024/12/30 16:0:2组卷:19引用:2难度:0.7844.氢气在氯气中燃烧时,破坏1mol H-H键消耗a kJ的能量,破坏1mol Cl-Cl键消耗b kJ的能量,形成1mol H-Cl键释放c kJ的能量。下列关系中正确的是( )
发布:2024/12/30 16:0:2组卷:27引用:2难度:0.6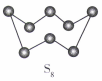 845.如图为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为。发布:2024/12/30 16:0:2组卷:19引用:4难度:0.7
845.如图为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为。发布:2024/12/30 16:0:2组卷:19引用:4难度:0.7846.有A、B、C、D四种元素,其原子序数依次增大,且质子数均小于18.A元素原子的最外层只有1个电子,该元素阳离子与N3-核外电子排布相同;B元素原子核外各轨道上均无成单电子:C元素原子的价电子排布为ns2np1,D-的核外电子构型与Ar相同。
(1)写出A、C、D的元素符号A,B,D。
(2)写出B元素原子的电子排布式,D元素原子的轨道表示。
(3)A、B、C、D第一电离能由小到大的顺序为(用元素符号表示,下同),电负性由小到大的顺序为。发布:2024/12/30 16:0:2组卷:16引用:2难度:0.5847.下列有关卤化氢的说法正确的是( )
发布:2024/12/30 16:0:2组卷:16引用:3难度:0.8848.(1)原子结构与元素周期表存在着内在联系.根据所学物质结构知识,请你回答下列问题:
①具有(n-1)d10ns2电子构型的元素位于周期表中区和族.
②日常生活中广泛应用的不锈钢,在其生产过程中添加了铬元素,该元素基态原子未
成对电子数为.
(2)等电子原理--原子总数相同、价电子总数相同的粒子具有相似的化学键特征,它们的许多性质是相近的.写出二种由多个原子组成的含有与N3-电子数相同的粒子的化学式、.这些粒子空间构型为.
(3)氯化亚砜(SOCl2)是一种很重要的化学试剂,可以作为氯化剂和脱水剂.氯化亚砜分子的VSEPR构型是;中心原子采取杂化方式.
(4)苏丹红颜色鲜艳、价格低廉,常被一些企业非法作为食品和化妆品等的染色剂,严重危害人们健康.苏丹红常见有Ⅰ、Ⅱ、Ⅲ、Ⅳ4种类型,苏丹红Ⅰ号的分子结构如图1所示.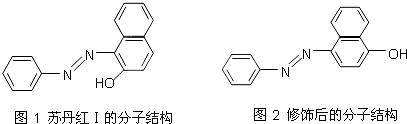
苏丹红Ⅰ在水中的溶解度很小,微溶于乙醇,有人把羟基取代在对位形成图2所示的结构,则其在水中的溶解度会(填“增大”或“减小”),原因是.发布:2024/12/30 16:0:2组卷:13引用:2难度:0.5849.原子结构与元素周期表存在着内在联系.请你回答下列问题:
(1)具有(n-1)d10ns2电子构型的元素位于周期表族;
(2)铁元素在周期表中的位置是;其原子核外电子排布式为;
(3)N层的s能级和p能级只有一个不成对电子的元素有多种.其中第一电离能最小的元素是(填元素符号,下同);电负性最大的元素是;外围电子排布为3d104s1的元素是.发布:2024/12/30 16:0:2组卷:21引用:2难度:0.3850.下列各说法中正确的是( )
发布:2024/12/30 16:0:2组卷:9引用:3难度:0.8



