回收利用含硫化合物有利于节约资源、保护环境。
(1)一种由含H2S的烟气回收硫黄的工艺为:将一部分含H2S的烟气在空气中燃烧,将燃烧所得产物与剩余烟气混合,冷却后可回收得到硫黄(S8)。该工艺中涉及反应为:
反应1:2H2S(g)+3O2(g)═2SO2(g)+2H2O(g)ΔH1=akJ•mol-1(a<0)
反应2:4H2S(g)+2SO2(g)═3S2(g)+4H2O(g)ΔH2=bkJ•mol-1(b>0)
反应3:4S2(g)═S8(s)ΔH3=ckJ•mol-1(c<0)
如果上述反应均能完全进行,为提高硫黄的产率,该工艺中需要控制反应1和反应2烟气的体积比为 1:21:2。
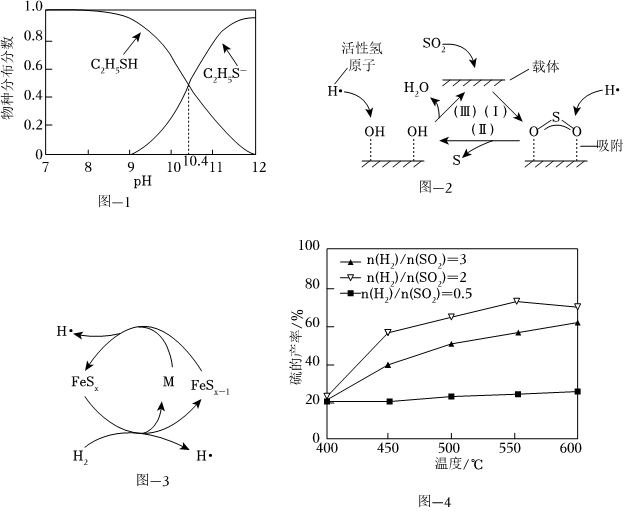
(2)某工业废水中含有乙硫醇(C2H5SH),已知C2H5SH水溶液中的物种分布分数如图1所示。已知:Ka1(H2S)=9×10-8,分别从电离常数和共价键极性的角度比较H2S和C2H5SH酸性强弱:
①酸性:H2S>C2H5SH酸性:H2S>C2H5SH(电离常数);
②酸性:H2S>C2H5SH酸性:H2S>C2H5SH(共价键极性)。
(3)一种以Al2O3为催化剂载体、FeS2为催化剂的H2还原烟气中SO2制S的反应机理如图-2和图-3所示:
①图-2中所示的转化过程可描述为 SO2吸附到催化剂载体上,在活性H原子的作用下,SO2中硫氧键断裂,H和O结合成OH吸附在载体上,同时有单质硫生成,H进一步与OH反应生成水SO2吸附到催化剂载体上,在活性H原子的作用下,SO2中硫氧键断裂,H和O结合成OH吸附在载体上,同时有单质硫生成,H进一步与OH反应生成水。
②图-3中FeSx和H2反应生成M、FeSx-1和H•的化学方程式为 FeSx+H2=M+S+FeSx-1+2H•FeSx+H2=M+S+FeSx-1+2H•。
③其他条件一定,改变起始时H2与SO2的比例,反应相同时间,测得S的产率与温度和n(H2)n(SO2)比值的关系如图-4所示。500℃时,n(H2)n(SO2)比值为3时硫的产率小于比值为2时的原因是 n(H2)n(SO2)比值为3时,氢气过量,过量的氢气进一步将S还原为H2S,导致S的产率减小n(H2)n(SO2)比值为3时,氢气过量,过量的氢气进一步将S还原为H2S,导致S的产率减小。
n
(
H
2
)
n
(
S
O
2
)
n
(
H
2
)
n
(
S
O
2
)
n
(
H
2
)
n
(
S
O
2
)
n
(
H
2
)
n
(
S
O
2
)
【考点】含硫物质的性质及综合应用.
【答案】1:2;酸性:H2S>C2H5SH;酸性:H2S>C2H5SH;SO2吸附到催化剂载体上,在活性H原子的作用下,SO2中硫氧键断裂,H和O结合成OH吸附在载体上,同时有单质硫生成,H进一步与OH反应生成水;FeSx+H2=M+S+FeSx-1+2H•;比值为3时,氢气过量,过量的氢气进一步将S还原为H2S,导致S的产率减小
n
(
H
2
)
n
(
S
O
2
)
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/7/28 8:0:9组卷:35引用:1难度:0.6
相似题
-
 1.硫俗称硫黄,主要存在于火山口附近或地壳的岩层中(如图),是一种黄色晶体,质脆易研成粉末,熔点为113℃,沸点为445℃,密度为2.06g/cm3。硫黄难溶于水,微溶于酒精、醚,易溶于二硫化碳。作为易燃固体,硫黄主要用于制造染料、农药、火柴、火药等。硫黄虽然是低毒性物质,但其燃烧后的气体对人体有致命的危害。
1.硫俗称硫黄,主要存在于火山口附近或地壳的岩层中(如图),是一种黄色晶体,质脆易研成粉末,熔点为113℃,沸点为445℃,密度为2.06g/cm3。硫黄难溶于水,微溶于酒精、醚,易溶于二硫化碳。作为易燃固体,硫黄主要用于制造染料、农药、火柴、火药等。硫黄虽然是低毒性物质,但其燃烧后的气体对人体有致命的危害。
(1)指出硫元素在元素周期表中的位置,硫元素的最高正价与最低负价分别是多少。
(2)从硫元素价态变化的角度分析,单质硫有哪些化学性质。
(3)如何用化学方法清洗试管内壁上附着的硫黄。写出反应的离子方程式。发布:2024/12/30 15:0:1组卷:6引用:2难度:0.7 -
2.下列说法不正确的是( )
发布:2024/12/30 15:0:1组卷:11引用:2难度:0.8 -
3.下列说法正确的是( )
发布:2024/12/30 15:0:1组卷:4引用:2难度:0.8


