 在容积为2.0L的密闭容器中,通入一定量的N2O4,发生反应:N2O4(g)⇌2NO2(g)。
在容积为2.0L的密闭容器中,通入一定量的N2O4,发生反应:N2O4(g)⇌2NO2(g)。
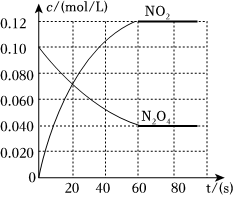
100℃时,各物质浓度随时间变化如图所示。
(1)60s内,v(N2O4)=0.001mol•L-1•s-10.001mol•L-1•s-1。
(2)下列叙述中,能说明该反应达到化学平衡状态的是 acac(填字母序号)。
A.NO2的生成速率是N2O4的生成速率的2倍
B.单位时间内消耗amolN2O4,同时生成2amolNO2
C.容器内的压强不再变化
D.容器内混合气体的密度不再变化
(3)降低温度,混合气体的颜色变浅,正反应是 吸热吸热反应(填“放热”或“吸热”)。
(4)欲提高N2O4的平衡转化率,理论上可以采取的措施为 BB。
A.增大压强
B.升高温度
C.加入催化剂
(5)100℃时,该反应的化学平衡常数的表达式为 K=c2(NO2)c(N2O4)K=c2(NO2)c(N2O4),数值为 0.360.36。
(6)平衡时,N2O4的转化率是 60%60%。
(7)100℃时,在容器中按初始浓度c(N2O4)=0.10mol/L、c(NO2)=0.10mol/L投料,反应 正向正向进行(填“正向”或“逆向”)。
c
2
(
N
O
2
)
c
(
N
2
O
4
)
c
2
(
N
O
2
)
c
(
N
2
O
4
)
【答案】0.001mol•L-1•s-1;ac;吸热;B;K=;0.36;60%;正向
c
2
(
N
O
2
)
c
(
N
2
O
4
)
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/25 1:0:1组卷:13引用:2难度:0.6
相似题
-
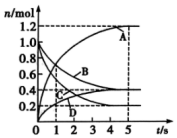 1.一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示。则下列对该反应的推断合理的是( )发布:2024/12/30 19:30:2组卷:32引用:3难度:0.7
1.一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示。则下列对该反应的推断合理的是( )发布:2024/12/30 19:30:2组卷:32引用:3难度:0.7 -
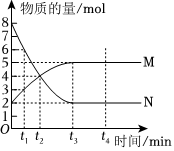 2.一定温度下,在容积为VL的密闭容器中进行反应:aN(g)⇌bM(g),M、N的物质的量随时间的变化曲线如图所示,下列说法错误的是( )发布:2024/12/30 14:30:1组卷:19引用:2难度:0.7
2.一定温度下,在容积为VL的密闭容器中进行反应:aN(g)⇌bM(g),M、N的物质的量随时间的变化曲线如图所示,下列说法错误的是( )发布:2024/12/30 14:30:1组卷:19引用:2难度:0.7 -
3.一定温度下,在容积为2L的密闭容器中,与同一个化学反应有关的A、B、C、D(其中A、B、C均为气体)四种物质的物质的量随反应时间的变化如图所示。E为该反应的另一种气态生成物,且在化学方程式中E的化学计量数与B的相同。请回答下列问题:
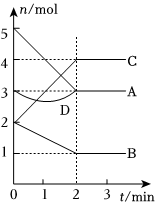
(1)该反应的反应物为。
(2)0~2min内,v(C)=,v(E)=。
(3)若降低温度,则v(正)(填“加快”、“减慢”或“不变”,下同),v(逆)。
(4)该反应达到平衡状态的标志有。(填序号)
a.A和C的物质的量相等
b.B的物质的量保持不变
c.A的正反应速率与B的逆反应速率之比为2:1
d.容器内压强不变
(5)物质D在反应中的作用是。发布:2024/12/30 14:30:1组卷:10引用:3难度:0.7


