电解原理在化学工业中有广泛应用。
(1)电解食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解示意图如图1所示,图中的阳离子交换膜只允许阳离子通过,请回答以下问题:

①电解饱和食盐水的总反应的离子方程式是 2Cl-+2H2O 通电 Cl2↑+H2↑+2OH-2Cl-+2H2O 通电 Cl2↑+H2↑+2OH-。
②精制饱和食盐水在b口加入的物质为 NaOHNaOH(写化学式)。
(2)全钒液流电池是一种新型的绿色环保储能系统,工作原理如图2:
通电
通电
| 离子种类 | VO + 2 |
VO2+ | V3+ | V2+ |
| 颜色 | 黄色 | 蓝色 | 绿色 | 紫色 |
V2+++2H+=V3++VO2++H2O
VO
+
2
V2+++2H+=V3++VO2++H2O
。VO
+
2
②当完成储能时,阴极溶液的颜色是
紫色
紫色
。(3)将PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示。

①写出电解时阴极的电极反应式
P
b
C
l
2
-
4
P
b
C
l
2
-
4
②电解过程中通过阳离子交换膜的离子主要为
H+
H+
。③电解过程中,Na2PbCl4电解液浓度不断减小,为了恢复其浓度,应该向
阴
阴
极室(填“阴”或者“阳”)加入 PbO
PbO
(填化学式)。【考点】电解原理;原电池与电解池的综合.
【答案】2Cl-+2H2O Cl2↑+H2↑+2OH-;NaOH;V2+++2H+=V3++VO2++H2O;紫色;+2e-=Pb+4Cl-;H+;阴;PbO
通电
VO
+
2
P
b
C
l
2
-
4
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/9/3 2:0:8组卷:58引用:5难度:0.5
相似题
-
1.铈(Ce)是镧系金属元素。空气污染物NO通常用含Ce4+的溶液吸收,生成HNO2、
,再利用电解法将上述吸收液中的HNO2转化为无毒物质,同时生成Ce4+,其原理如图所示。下列说法正确的是( )NO-3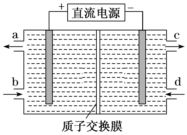 发布:2025/1/6 7:30:5组卷:129引用:7难度:0.7
发布:2025/1/6 7:30:5组卷:129引用:7难度:0.7 -
2.(NH4)2S2O8电化学循环氧化法可用于废水中苯酚的降解,示意图如图。
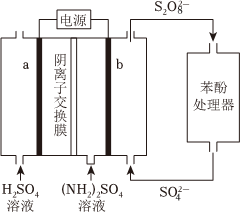
(1)(NH4)2S2O8的电解法制备。
已知:电解效率η的定义为η(B)=×100%。n(生成B所用的电子)n(通过电极的电子)
①电极b是极。
②生成S2的电极反应式是O2-8。
③向阳极室和阴极室各加入100mL溶液。制备S2的同时,还在电极b表面收集到2.5×10-4mol气体,气体是O2-8。经测定η(S2)为80%,不考虑其他副反应,则制备的(NH4)2S2O8的物质的量浓度为O2-8mol/L。
(2)苯酚的降解
已知:•具有强氧化性,Fe2+性度较高时会导致SO-4•猝灭。S2SO-4可将苯酚氧化为CO2,但反应速率较慢。加入Fe2+可加快反应,过程为:O2-8
i.S2+Fe2+═O2-8+SO2-4•+Fe3+SO-4
ii.•将苯酚氧化SO-4
①•氧化苯酚的离子方程式是SO-4。
②将电解得到的含S2溶液稀释后加入苯酚处理器,调节溶液总体积为1L,pH=1,测得在相同时间内,不同条件下苯酚的降解率如图。O2-8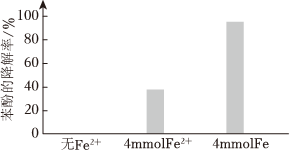
用等物质的量的铁粉代替FeSO4,可明显提高苯酚的降解率,主要原因是。
(3)苯酚残留量的测定
已知:电解中转移1mol电子所消耗的电量为F库仑。
取处理后的水样100mL,酸化后加入KBr溶液,通电。电解产生的Br2全部与苯酚反应,当苯酚完全反应时,消耗的电量为a库仑,则样品中苯酚的含量为g/L。(苯酚的摩尔质量:94g/mol)发布:2024/12/30 11:30:1组卷:165引用:3难度:0.4 -
3.如图所示,某同学设计一个甲醚(CH3OCH3)燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
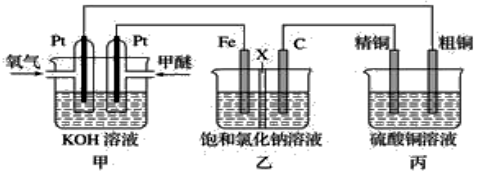
(1)通入氧气的电极为极,写出负极电极反应式。
(2)铁电极为极,石墨电极(C)的电极反应式为。
(3)反应一段时间后,乙装置中生成NaOH主要在(填“铁极”或“石墨极”)区。
(4)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为,反应一段时间,硫酸铜溶液浓度将(填“增大”、“减小”或“不变”)发布:2025/1/3 8:0:1组卷:6引用:1难度:0.6


