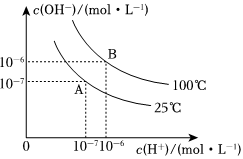
 在水的电离平衡中,c(H+)和c(OH-)的关系如图所示:
在水的电离平衡中,c(H+)和c(OH-)的关系如图所示:
(1)A点水的离子积为1×10-4,B点水的离子积为 10-1210-12.
造成水的离子积变化的原因是 水的电离是吸热反应,升高温度促进电离,所以水的离子积常数增大水的电离是吸热反应,升高温度促进电离,所以水的离子积常数增大.
(2)100℃时,0.01mol/LNaOH溶液的pH=1010.
(3)100℃时,将pH=11的NaOH溶液与pH=2的稀盐酸混合,欲使混合溶液呈中性,则NaOH溶液与盐酸体积比为 1:101:10.
【考点】水的电离;酸碱混合时的定性判断及有关pH的计算.
【答案】10-12;水的电离是吸热反应,升高温度促进电离,所以水的离子积常数增大;10;1:10
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/8/16 15:0:1组卷:55引用:4难度:0.3


