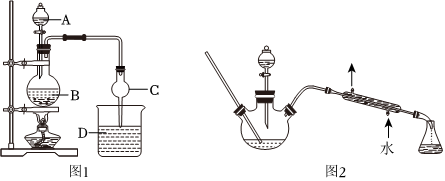
乙酸乙酯是食用香精中用量较大的合成香料之一,大量用于调配香蕉、梨、桃、菠萝、葡萄等香型食用香精。某化学兴趣小组设计的制备乙酸乙酯的装置如图1所示。
查阅资料知:
Ⅰ.CaCl2可与乙醇反应生成不溶于有机溶剂而溶于水的结晶醇化物。
Ⅱ.有关数据如表所示:
| 物质 | 乙醇 | 乙酸 | 乙酸乙酯 | 浓硫酸(98%) |
| 沸点/℃ | 78.5 | 117.9 | 77.0 | 338.0 |
①如图所示,连接好装置(装置气密性良好),在100mL圆底烧瓶内加入碎瓷片后,加入15mL乙醇,然后边振荡圆底烧杯边慢慢加入10mL98%的浓硫酸,冷却后,通过分液漏斗(A)向圆底烧瓶(B)内慢慢加入12mL乙酸、在烧杯D中加入饱和Na2CO3溶液。
②点燃酒精灯,用小火均匀加热装有混合溶液的圆底烧瓶。
③待D中收集到一定量产物后停止加热,撤出C,将D中混合物搅拌,然后静置分层。
④分离出乙酸乙酯层、洗涤、干燥。
请回答下列问题:
(1)碎瓷片的作用是
防止液体暴沸
防止液体暴沸
、浓硫酸的作用是 作催化剂和吸水剂
作催化剂和吸水剂
。若用同位素示踪法来确定产物水分子中氧原子的提供者,请写出能表示18O位置的制取乙酸乙酯的化学方程式:CH3CO18OH+CH3CH2OHCH3COOCH2CH3+O(或CH3COOH+CH3OHCH3CO18OCH2CH3+H2O)
浓硫酸
△
H
18
2
CH
18
2
浓硫酸
△
CH3CO18OH+CH3CH2OHCH3COOCH2CH3+O(或CH3COOH+CH3OHCH3CO18OCH2CH3+H2O)
。浓硫酸
△
H
18
2
CH
18
2
浓硫酸
△
(2)仪器C的名称是
球形干燥管
球形干燥管
,其作用是加速乙酸乙酯冷凝和 防止倒吸
防止倒吸
。(3)D中饱和Na2CO3溶液的作用是
除去乙酸;溶解乙醇;降低乙酸乙酯的溶解度,有利于分层
除去乙酸;溶解乙醇;降低乙酸乙酯的溶解度,有利于分层
。(4)步骤②中需要小火均匀加热的理由主要是
减少乙酸和乙醇的挥发,提高其转化率,并防止副反应的发生
减少乙酸和乙醇的挥发,提高其转化率,并防止副反应的发生
。(5)写出步骤(3)中观察到的现象:
溶液上层有油状液体生成,有果香味
溶液上层有油状液体生成,有果香味
。分离出乙酸乙酯层后,一般用饱和食盐水和饱和氯化钙溶液洗涤乙酸乙酯层,可除去 碳酸钠、乙醇、乙酸钠
碳酸钠、乙醇、乙酸钠
(填名称)杂质。(6)该小组成员又设计了如图2所示的制取乙酸乙酯的装置(夹持装置、加热装置圴已略去),与如图1所示的装置相比,本装置的主要优点是
冷凝管的冷却效果比空气冷凝的效果好;能控制加热的温度,减少副反应的发生,提高产率(合理即可)
冷凝管的冷却效果比空气冷凝的效果好;能控制加热的温度,减少副反应的发生,提高产率(合理即可)
。【考点】乙酸乙酯的制取.
【答案】防止液体暴沸;作催化剂和吸水剂;CH3CO18OH+CH3CH2OHCH3COOCH2CH3+O(或CH3COOH+CH3OHCH3CO18OCH2CH3+H2O);球形干燥管;防止倒吸;除去乙酸;溶解乙醇;降低乙酸乙酯的溶解度,有利于分层;减少乙酸和乙醇的挥发,提高其转化率,并防止副反应的发生;溶液上层有油状液体生成,有果香味;碳酸钠、乙醇、乙酸钠;冷凝管的冷却效果比空气冷凝的效果好;能控制加热的温度,减少副反应的发生,提高产率(合理即可)
浓硫酸
△
H
18
2
CH
18
2
浓硫酸
△
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/7/1 8:0:9组卷:98引用:1难度:0.5
相似题
-
1.下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务.
【实验目的】制取乙酸乙酯
【实验原理】甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯.
【装置设计】甲、乙、丙三位同学分别设计了下列三套实验装置:
请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,较合理的是(选填“甲”或“乙”).丙同学将甲装置进行了改进,将其中的玻璃管改成了球形干燥管,除起冷凝作用外,另一重要作用是.
【实验步骤】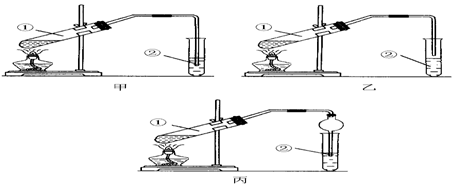
(1)按丙同学选择的装置组装仪器,在试管中先加入3mL乙醇,并在摇动下缓缓加入2mL浓硫酸充分摇匀;冷却后再加入2mL冰醋酸;
(2)将试管固定在铁架台上;
(3)在试管②中加入适量的饱和Na2CO3溶液;
(4)用酒精灯对试管①加热;
(5)当观察到试管②中有明显现象时停止实验.
【问题讨论】
a.步骤(1)安装好实验装置,加入样品前还应检查;
b.写出试管①发生反应的化学方程式(注明反应条件);
c.试管②中饱和Na2CO3溶液的作用是;
d.从试管②中分离出乙酸乙酯的实验操作是.发布:2024/12/30 19:30:2组卷:43引用:7难度:0.5 -
2.在酯化反应实验中制得的乙酸乙酯中混有少量的乙酸,应选用下列哪种试剂洗涤除去( )
发布:2024/12/30 8:30:1组卷:39引用:3难度:0.9 -
3.乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室利用如图A装置制备乙酸乙酯。
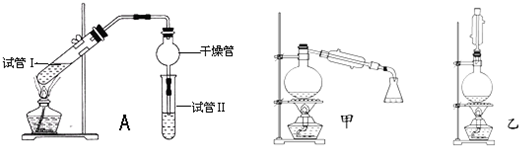
(1)若实验中用乙酸和含18O的乙醇作用,该反应的化学方程式是:。与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是。
(2)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管Ⅱ再测有机层的厚度,实验记录如下:
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是实验编号 试管Ⅰ中试剂 试管Ⅱ中试剂 有机层的厚度/cm A 2mL乙醇、1mL乙酸、
1mL 18mol•L-1浓硫酸饱和Na2CO3溶液 3.0 B 2mL乙醇、1mL乙酸 0.1 C 2mL乙醇、1mL乙酸、
3mL 2mol•L-1H2SO40.6 D 2mL乙醇、1mL乙酸、盐酸 0.6 mL和mol•L-1。
②分析实验(填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率。
(3)若现有乙酸90g,乙醇138g发生酯化反应得到88g乙酸乙酯,试计算该反应的产率为。
(4)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,如图是分离操作步骤流程图。图中内为适当的试剂,内为适当的分离方法。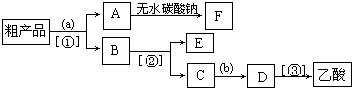
①试剂a是;分离方法②是,分离方法③是。分离方法①是分液,在具体操作中应充分振荡,然后静置,待分层后(填标号)。
A.直接将乙酸乙酯从分液漏斗上口倒出
B.直接将乙酸乙酯从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸乙酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸乙酯从上口放出
②在得到的A中加入无水碳酸钠粉末,振荡,目的是。
(5)为充分利用反应物,甲、乙两位同学分别设计了如图甲、乙两个装置(乙同学待反应完毕冷却后,再用饱和碳酸钠溶液提取烧瓶中的产物)。你认为最合理的是。发布:2024/12/30 19:0:1组卷:84引用:3难度:0.1


