以天然石膏(主要成分CaSO4,杂质MgSO4等)为原料可制备硫酸铵和氯化钙。
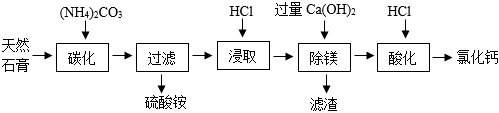
(1)“碳化”中发生反应的化学方程式有:(NH4)2CO3+CaSO4═CaCO3↓+(NH4)2SO4和 (NH4)2CO3+MgSO4=MgCO3↓+(NH4)2SO4(NH4)2CO3+MgSO4=MgCO3↓+(NH4)2SO4。写出硫酸铵的一种用途:作氮肥作氮肥。
(2)“浸取”中所发生化学反应的反应类型是 复分解复分解反应。为了提高“浸取”的效果,可采取的措施有:适当升高温度、适当增大盐酸浓度、边加盐酸边搅拌、增加酸浸时间等适当增大盐酸浓度、边加盐酸边搅拌、增加酸浸时间等。
(3)“除镁”中发生反应的化学方程式为 Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2。
(4)用盐酸“酸化”的目的是 将溶液中的过量Ca(OH)2转化为CaCl2(合理即可)将溶液中的过量Ca(OH)2转化为CaCl2(合理即可)。
【考点】物质的相互转化和制备.
【答案】(NH4)2CO3+MgSO4=MgCO3↓+(NH4)2SO4;作氮肥;复分解;适当增大盐酸浓度、边加盐酸边搅拌、增加酸浸时间等;Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2;将溶液中的过量Ca(OH)2转化为CaCl2(合理即可)
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2026/2/5 0:30:1组卷:32引用:1难度:0.4


