2021年3月全国两会期间,政府工作报告中提到的“碳达峰”“碳中和”成为热词。“碳中和”指的是测算在一定时间内直接或间接产生的二氧化碳或温室气体排放总量,通过植树造林、节能减排等形式,抵消自身产生的二氧化碳排放,实现二氧化碳的“零排放”。温室气体二氧化碳与氢气反应制备燃料甲醇的技术,能促进“碳中和”。请完成下列问题:CO2加氢制甲醇的总反应可表示为:CO2 (g)+3H2(g)⇌CH3OH(g)+H2O(g)ΔH=?kJ⋅mol-1
该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH1=+42kJ⋅mol-1
②2CO(g)+2H2(g)⇌CH3OH(g) ΔH2=-90kJ⋅mol-1
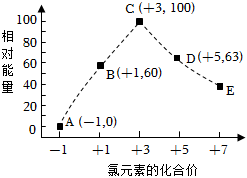
(1)总反应的ΔH=-48-48kJ⋅mol-1;若反应①为慢反应,如图1示意图中能体现上述反应能量变化的是 BB(填标号)。

(2)合成总反应在起始物n(H2)n(CO2)=3时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在t=250°C下的x(CH3OH)~p、在p=5×105Pa下的x(CH3OH)~t如图2所示。

①图中对应等温过程的曲线是 aa,判断的理由是 总反应为气体分子数减小的反应,温度一定时增大压强,平衡向正反应方向移动,甲醇的物质的量分数变大,曲线斜率为正总反应为气体分子数减小的反应,温度一定时增大压强,平衡向正反应方向移动,甲醇的物质的量分数变大,曲线斜率为正。
②当x(CH3OH)=0.10时,CO2的平衡转化率α=33.3%33.3%(保留三位有效数字),反应条件可能为 5×105Pa、210°C5×105Pa、210°C或 9×105Pa、250°C9×105Pa、250°C。
n
(
H
2
)
n
(
C
O
2
)
【答案】-48;B;a;总反应为气体分子数减小的反应,温度一定时增大压强,平衡向正反应方向移动,甲醇的物质的量分数变大,曲线斜率为正;33.3%;5×105Pa、210°C;9×105Pa、250°C
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/8/2 8:0:9组卷:26引用:2难度:0.5