高铁酸钾(K2FeO4)是一种新型高效多功能绿色净水处理剂,其一种制备方法如图所示:
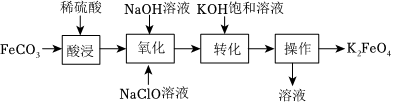
(1)“酸浸”时发生反应的化学方程式为 FeCO3+H2SO4=FeSO4+H2O+CO2↑FeCO3+H2SO4=FeSO4+H2O+CO2↑。
(2)“氧化”时FeSO4与NaOH、NaClO反应转化为Na2FeO4。
①Na2FeO4中铁元素的化合价为 +6+6。
②不同温度和pH下FeO2-4在水溶液中的稳定性如图所示。
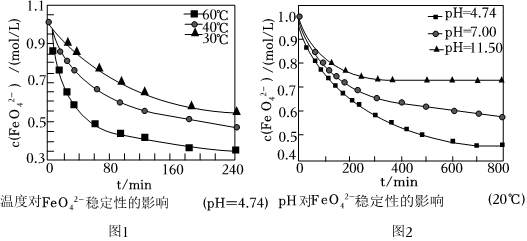
图1、图2中纵坐标表示单位体积内FeO2-4离子数目的多少,数值越小,表明FeO2-4离子数目越少,在该条件下越不稳定。为了提高“合成”时Na2FeO4的产率,控制反应适宜的条件是 30℃,pH=11.530℃,pH=11.5。该过程中需加入过量NaOH,其目的是 使硫酸亚铁完全反应;使溶液成碱性,防止高铁酸钠分解使硫酸亚铁完全反应;使溶液成碱性,防止高铁酸钠分解。
(3)“转化”时加入饱和KOH溶液,即可析出K2FeO4晶体,写出反应的化学方程式为 Na2FeO4+2KOH=2NaOH+K2FeO4↓Na2FeO4+2KOH=2NaOH+K2FeO4↓。
(4)“操作”的名称是 过滤过滤;洗涤K2FeO4晶体时,用酒精而不用蒸馏水的优点:①减少晶体溶解损耗;②酒精据挥发性酒精据挥发性。
(5)K2FeO4净水时生成的胶状物具有疏松多孔的网状结构,可 吸附吸附悬浮于水中的杂质,使之从水中沉降出来。
(6)K2FeO4的纯度与烘干温度的关系如下表,80℃时铁元素的存在形式为 Fe2O3Fe2O3(填化学式)。
不同温度所得产品特性:
F
e
O
2
-
4
F
e
O
2
-
4
F
e
O
2
-
4
| 干燥温度/℃ | 纯度/% | 产品颜色 |
| 25 | 92.5 | 紫红色 |
| 60 | 98.3 | 紫黑色 |
| 80 | 0 | 红色 |
【答案】FeCO3+H2SO4=FeSO4+H2O+CO2↑;+6;30℃,pH=11.5;使硫酸亚铁完全反应;使溶液成碱性,防止高铁酸钠分解;Na2FeO4+2KOH=2NaOH+K2FeO4↓;过滤;酒精据挥发性;吸附;Fe2O3
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/6/26 8:0:9组卷:102引用:1难度:0.5
相似题
-
1.新冠肺炎疫情防控期间,西安市各学校开展全域喷洒低浓度、有效成分是次氯酸钠的“84”消毒液进行消毒。如图所示是模拟制备“84”消毒液的流程(Cl2是一种黄绿色的有毒气体)。请回答下列问题:
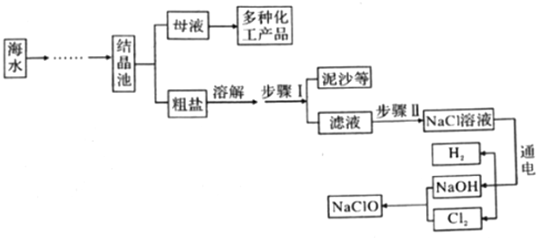
(1)NaOH的俗称为(写一种)。
(2)步骤Ⅱ中,通常用碳酸钠溶液除去滤液中的氯化钙杂质,请写出有关反应的化学方程式。
(3)电解水时,一般在水中加入少量NaOH以增强水的导电性,不能加入NaCl的原因是。发布:2025/1/3 8:0:1组卷:6引用:1难度:0.5 -
2.某种家用的消毒液的主要成分是次氯酸钠(NaClO),制取NaClO的化学方程式为:Cl2+2NaOH=NaClO+NaCl+H2O,下列说法错误的是( )
发布:2025/1/3 8:0:1组卷:71引用:1难度:0.7 -
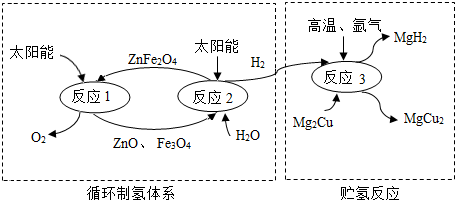 3.如图是制取与贮存氢气的一种方法,Mg2Cu是一种贮氢合金,吸氢后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列说法不正确的是( )发布:2024/12/31 8:0:1组卷:48引用:2难度:0.5
3.如图是制取与贮存氢气的一种方法,Mg2Cu是一种贮氢合金,吸氢后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列说法不正确的是( )发布:2024/12/31 8:0:1组卷:48引用:2难度:0.5


