化学反应过程中,不仅有物质的变化,同时还伴随能量变化。研究化学反应中的能量变化有重要意义。
(1)下列反应中属于吸热反应的是 DD。
A.氢气燃烧
B.铝粉和氧化铁粉末的反应
C.浓硫酸稀释
D.Ba(OH)2⋅8H2O和NH4Cl固体的反应
(2)已知充分燃烧1mol乙炔气体(分子式为C2H2)时生成二氧化碳气体和液态水,并放出热量bkJ,则乙炔燃烧的热化学方程式正确的是 CC。
A.C2H2+52O2=2CO2+H2O ΔH=-bkJ/mol
B.2C2H2+5O2=4CO2+2H2O ΔH=-2bkJ/mol
C.C2H2(g)+52O2(g)=2CO2(g)+H2O(l) ΔH=-bkJ/mol
D.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH=2bkJ/mol
(3)分别取40mL0.50mol/L的盐酸与40mL0.55mol/L的氢氧化钠溶液混合进行中和热的测定,下列说法正确的是 BB。
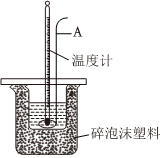
A.仪器A是金属搅拌棒
B.稍过量的氢氧化钠是确保盐酸完全反应
C.酸碱混合时,NaOH溶液应缓缓倒入小烧杯中,不断搅拌
D.用氢氧化钡和硫酸代替氢氧化钠和盐酸溶液,结果也是正确的
(4)下列说法正确的是 CC。
A.焓变或熵变均可以单独作为反应自发性的判据
B.能自发进行的反应一定能迅速发生
C.ΔH<0、ΔS<0的反应在低温时能自发进行
D.两种物质反应,无论方程式的书写形式如何,ΔH均不变
(5)如图是某化学反应中的能量变化图。
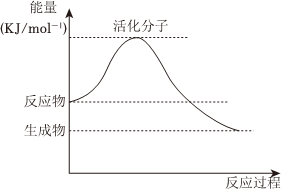
①该反应是 放热放热(填“吸热”或“放热”)反应。
②请在图中标注出该反应的活化能E 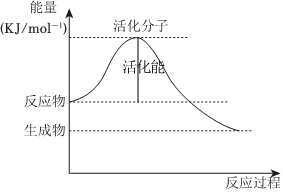
 。
。
(6)298K,100KPa时,把1molH2和1molI2放在某密闭容器中进行反应,热化学方程式如下:H2(g)+I2(g)⇌2HI(g) ΔH=-9kJ/mol,测得反应放出的热量总是少于9kJ/mol,其原因是 该反应是可逆反应该反应是可逆反应。
5
2
5
2


【答案】D;C;B;C;放热; ;该反应是可逆反应
;该反应是可逆反应
 ;该反应是可逆反应
;该反应是可逆反应【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/7/11 8:0:9组卷:61引用:1难度:0.5



