 直接甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源.
直接甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源.
(1)101kPa时,1mol CH3OH完全燃烧生成稳定的氧化物放出热量726.51kJ/mol,则甲醇燃烧的热化学方程式为CH3OH(l)+32O2(g)=CO2(g)+2H2O(l)△H=-726.51kJ/molCH3OH(l)+32O2(g)=CO2(g)+2H2O(l)△H=-726.51kJ/mol.
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H1=+49.0kJ•mol-1
②CH3OH(g)+12O2(g)=CO2(g)+2H2(g)△H2
已知H2(g)+12O2(g)═H2O(g)△H=-241.8kJ•mol-1
则反应②的△H2=-192.8kJ•mol-1-192.8kJ•mol-1.
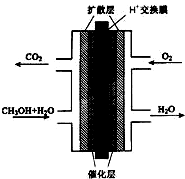
(3)甲醇燃料电池的结构示意图如右.甲醇进入负负极(填“正”或“负”),该极发生的电极反应为CH3OH+H2O-6e-=CO2+6H+CH3OH+H2O-6e-=CO2+6H+.
(4)已知H-H键能为436kJ/mol,H-N键能为391kJ/mol,根据化学方程式:
N2(g)+3H2(g)=2NH3(g)△H=-92.4KJ/mol,则N≡N键的键能是945.6KJ/mol945.6KJ/mol.
3
2
3
2
1
2
1
2
【答案】CH3OH(l)+O2(g)=CO2(g)+2H2O(l)△H=-726.51kJ/mol;-192.8kJ•mol-1;负;CH3OH+H2O-6e-=CO2+6H+;945.6KJ/mol
3
2
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/5/27 14:0:0组卷:17引用:3难度:0.5
相似题
-
1.氢在地球上主要以化合态的形式存在,是宇宙中分布最广泛的物质,它构成了宇宙质量的75%,属于二次能源.工业上生产氢的方式很多,常见的有水电解制氢,煤炭气化制氢,重油及天然气水蒸气催化制氢等.氢气是一种理想的绿色能源,如图1为氢能产生和利用的途径:
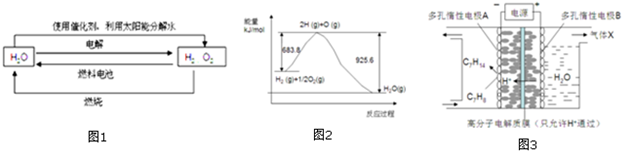
(1)图1的四个过程中能量转化形式有
A.2种 B.3种 C.4种 D.4种以上
(2)电解过程要消耗大量的电能,而使用微生物作催化剂在阳光下也能分解水.
2H2O(1)2H2(g)+O2(g)△H 1 2H2O(1)通电2H2(g)+O2(g)△H2光照催化剂
以上反应的△H1△H2(选填“<”、“>”或“=”)
(3)已知H2O(l)→H2O(g)△H=+44kJ.mol-1,依据图2能量变化写出氢气燃烧生产液态水的热化学方程式
(4)氢能利用需要选择合适的储氢材料.
①NaBH4是一种重要的储氢载体,能与水反应生成NaBO2,且反应前后B的化合价不变,该反应的化学方程式为
②镧镍合金在一定条件下可吸收氢气生产氢化物:LaNi3(s)+3H2(g)═LaNi3H6(s)△H<0,欲使LaNi3H6(s)释放出气态氢,根据平衡移动的原理,可改变的条件之一是
③一定条件下,如图3所示装置可实现有机物的电化学储氢,使C7H8转化为C7H14,则电解过程中产生的气体X 为,电极A上发生的电极反应式为.发布:2024/12/17 8:0:2组卷:38引用:1难度:0.5 -
2.肼(N2H4)可作为发射火箭的燃料。已知1g液态肼(N2H4)气体在空气中燃烧生成氮气和水蒸气,放出16.7kJ的热量,该反应的热化学方程式是( )
发布:2024/12/30 3:0:4组卷:121引用:9难度:0.6 -
3.在298K、1.01×105Pa下,将0.5mol CO2通入750mL 1mol•L-1NaOH溶液中充分反应,测得反应放出xkJ的热量。已知在该条件下,1mol CO2通入1L 2mol•L-1NaOH溶液中充分反应放出ykJ的热量,则CO2与NaOH溶液反应生成NaHCO3的热化学方程式正确的是( )
发布:2024/12/30 4:0:1组卷:143引用:5难度:0.7


