某校化学兴趣小组的同学发现长期露置在空气中的金属M表面会被锈蚀,于是他们一起探究金属M锈蚀的原因。经检测,锈蚀物中除含有M元素外,还含有C、H、O三种元素。他们分析与金属M发生反应生成锈蚀物的物质。请你参与并回答:
推测Ⅰ:(1)根据锈蚀产物的组成元素,可推测空气中的H2O、CO2H2O、CO2肯定参加了反应。
推测Ⅱ:由于锈蚀产物中的O元素可能有多种来源,因此不能确定空气中的氧气是否参加了反应。
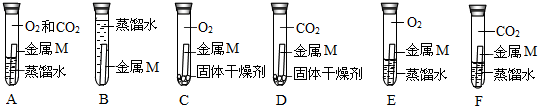
(2)为了验证空气中的氧气是否参加了反应,设计了如下系列实验(见图),你认为其中必须要做的实验是AFAF(填实验编号)。(说明①所用蒸馏水是煮沸迅速冷却的②固体干燥剂吸收水分,不吸收二氧化碳和氧气。)实验的结果是氧气参加了反应。
(3)若金属M是铜,铜器长期露置在空气中会生成铜绿,它的主要成分是碱式碳酸铜,化学式为Cu2(OH)2CO3,试写出铜在空气中锈蚀的化学反应方程式2Cu+O2+H2O+CO2=Cu2(OH)2CO32Cu+O2+H2O+CO2=Cu2(OH)2CO3
(4)兴趣小组同学发现实验室一片久置的铜片表面附着有一层绿色固体,查阅资料得知绿色固体是铜绿[化学式为Cu2(OH)2CO3],甲同学从铜片上刮下一些铜绿进行如下探究,请填写表中空白:
| 实验步骤 | 实验现象 | 实验结论 |
取少量铜绿在图装置中加热。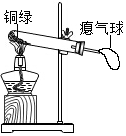 |
试管内壁有水雾。 | ①铜绿加热产生 水 水 。 |
| ② 试管中的固体变黑色 试管中的固体变黑色 。 |
铜绿加热后生成氧化铜。 | |
|
气球胀大。 |
有气体生成 有气体生成
|
【考点】探究金属锈蚀的条件.
【答案】H2O、CO2;AF;2Cu+O2+H2O+CO2=Cu2(OH)2CO3;水;试管中的固体变黑色;有气体生成
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/8/29 16:0:8组卷:75引用:5难度:0.5
相似题
-
 1.在进行“二氧化碳制取和性质实验”时,小明发现放置小蜡烛的铜架上出现了绿色物质,且绿色物质只出现在下部(伸到烧杯下面的部分),上部和在烧杯外的部分没有出现,小明思考,铜也会生锈吗?为什么只出现在下部呢?铜生锈的条件是什么?
1.在进行“二氧化碳制取和性质实验”时,小明发现放置小蜡烛的铜架上出现了绿色物质,且绿色物质只出现在下部(伸到烧杯下面的部分),上部和在烧杯外的部分没有出现,小明思考,铜也会生锈吗?为什么只出现在下部呢?铜生锈的条件是什么?
【查阅资料】铜在一定条件下会锈蚀生成一种绿色的物质(铜绿),其主要成分是碱式碳酸铜,化学式时候Cu2(OH)2CO3,受热易分解.
【猜想与假设】依据铜绿的化学式,小明猜想铜生锈的条件可能是,铜与氧气、共同作用,做出此猜想的依据是.
【设计实验】将四块铜片分别按如图放置半个月,观察现象如下,A中铜片生锈且水面附近锈蚀最严重,B、C、D中铜片不生锈,D装置中氢氧化钠溶液的作用是,写出该反应的化学方程式.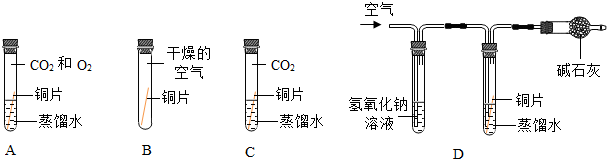
【得出结论】根据A和D中的实验现象可知铜生锈需要.
【反思与应用】利用所得结论填空,依据本实验结合“二氧化碳浇灭蜡烛”的实验操作推测铜架下部容易生锈的原因是.
【实验拓展】有资料显示,氧化铜也能加快过氧化氢溶液的分解速率.
(1)给你一支已经产生铜绿的铜架,5%过氧化氢溶液,请你设计实验证明(仪器自选).
(2)请你试着写出铜生成铜绿的化学方程式.发布:2024/11/10 8:0:1组卷:53引用:1难度:0.3 -
2.化学小组对钢铁的锈蚀进行实验研究。
Ⅰ.探究钢铁锈蚀的基本条件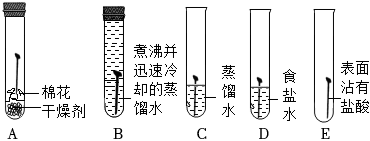
(1)一段时间后,C、D、E中铁钉生锈,A、B中铁钉无明显锈蚀。由A、B、C的现象可知,铁的锈蚀是铁跟等物质作用的过程。
(2)使用自来水重新进行如图实验,一段时间后发现试管B中铁钉生锈了,其可能的原因是。
Ⅱ.探究食盐水浓度对钢铁腐蚀速率的影响
用如图装置进行实验,每组实验加入铁炭总质量为24g,食盐水体积为7.5mL,恰好能将固体润湿。测得的数据见下表:(提供资料:示数差3cm是指U型管左侧液面上升3cm。)
(3)分析食盐水浓度对钢铁腐蚀速率的影响应对比实验序号 铁炭质量比 食盐水浓度/% 示数差3cm所用时间/s 10分钟时温度升高值/℃ 实验① 2:1 26 90 7.8 实验② 4:1 26 170 4.2 实验③ 6:1 26 190 3.3 实验④ 2:1 13 140 6 实验⑤ 2:1 6.5 140 6 (填实验序号)。有同学提出应该再加一组实验,研究铁炭质量比为2:1、食盐水浓度为3.3%时的实验数据,你觉得是否有必要,并说明理由。
(4)查阅资料得知,食盐水中的氯离子能破坏钢筋表面的钝化膜,并促使铁发生一系列反应得到氢氧化铁,它在空气中风化失水后变成氧化铁。钢筋锈蚀过程中生成氧化铁的反应方程式是。
Ⅲ.探究水样的pH及溶解氧浓度对钢铁腐蚀速率的影响
步骤1:按如图连接好装置,检查装置气密性。
步骤2:向三颈烧瓶中放入3.5g生铁粉末,向分液漏斗内加入10mL不同浓度的稀盐酸。
步骤3:将稀盐酸全部注入三颈烧瓶内,关闭分液漏斗活塞,一段时间后,至恢复到室温时,采集的数据见下表: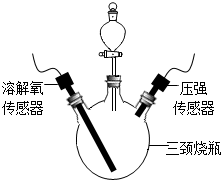
(5)步骤1中检查装置气密性的方法为:先在分液漏斗中加水,再打开活塞,观察到序号 盐酸pH P反应前 P反应后 DO反应前 DO反应后 开始降低所需时间/s 实验① 2.0 90.8 91.8 5.2 4.3 131 实验② 3.0 90.8 91.5 5.0 3.7 68 实验③ 4.0 90.8 90.3 4.9 3.4 24 实验④ 5.0 90.8 90.5 4.9 3.7 98 实验⑤ 6.0 90.8 90.6 4.4 3.7 175 (填现象),表明装置的气密性良好。
(6)实验①和实验②反应后压强变大。进行实验③时,观察到溶液中有气泡冒出,反应后体系内压强却变小了,变小的原因是。
(7)分析表中数据,在该实验条件下,下列说法正确的有(填字母)。
a.当pH=2时,铁粉与氧气的锈蚀速率最快
b.稀盐酸中的溶解氧含量与盐酸的pH有关
c.铁粉和盐酸,氧气在刚接触时不是同时发生反应发布:2024/12/24 10:30:2组卷:219引用:4难度:0.5 -
3.化学小组对钢铁的锈蚀进行实验研究。
Ⅰ.探究钢铁锈蚀的基本条件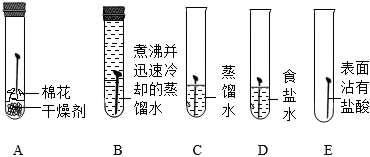
(1)一段时间后,C、D、E中铁钉生锈,A、B中铁钉无明显锈蚀。由A、B、C的现象可知,铁的锈蚀是铁跟(填化学式)等物质作用的过程。D中铁钉比C中铁钉锈蚀程度严重,说明。
(2)使用自来水重新进行如图实验,一段时间后发现试管B中铁钉生锈了,其可能的原因是。
Ⅱ.探究食盐水对钢铁腐蚀速率的影响
用如图装置进行实验,锥形瓶中放生铁粉末,滴管中预先加入2mL不同浓度的食盐水,并用氧气传感器测定锥形瓶内的氧气浓度,数据如下表所示: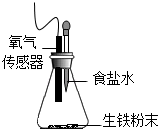
(3)该实验探究的是实验组 生铁粉末质量 食盐水浓度 3min时瓶内氧气浓度 实验① 3.5g 4% 18.96% 实验② 3.5g 8% 18.56% 实验③ 3.5g 16% 18.28% 实验④ 3.5g 24% 17.99% 对钢铁腐蚀速率的影响,其实验结论是。
(4)查阅资料得知,食盐水中的氯离子能破坏钢筋表面的钝化膜(其原理如图所示),并促使铁发生一系列反应得到Fe(OH)3,Fe(OH)3在空气中风化失水后变成氧化铁。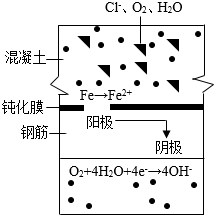
①氯离子破坏钢筋表面的钝化膜的过程中,从阳极向阴极转移的微粒是。
②钢筋锈蚀过程中得到氧化铁的反应方程式为。
Ⅲ.探究水样的pH及溶解氧浓度对钢铁腐蚀速率的影响
步骤1:按如图连接好装置,检查装置气密性。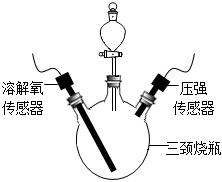
步骤2:向三颈烧瓶中放入3.5g生铁粉末,向分液漏斗内加入10mL不同浓度的稀盐酸。
步骤3:将盐酸全部注入三颈烧瓶内,关闭分液漏斗活塞,同时采集数据见下表:
(5)步骤1中检查装置气密性的方法为序号 盐酸pH 压强p/kPa 溶解氧/mg•L-1 p反应前 p反应后 DO反应前 DO反应后 开始降低所需时间/s 实验① 2.0 90.8 91.8 5.2 4.3 131 实验② 3.0 90.8 91.5 5.0 3.7 68 实验③ 4.0 90.8 90.3 4.9 3.4 24 实验④ 5.0 90.8 90.5 4.9 3.7 98 实验⑤ 6.0 90.8 90.6 4.4 3.7 175 。
(6)实验1和实验2反应后压强变大的主要原因是(用化学方程式表示)。
(7)进行实验3时,观察到溶液中有气泡冒出,反应后体系内压强却变小了。其原因是。
(8)分析表中数据,在该实验条件下,下列说法正确的有。
A.当pH=2时,铁粉与氧气的锈蚀速率最快
B.稀盐酸中的溶解氧含量与盐酸的pH有关
C.铁粉和盐酸,氧气的反应可以同时发生发布:2024/12/25 12:0:1组卷:258引用:3难度:0.7


