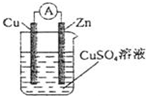
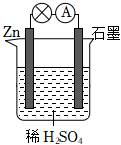
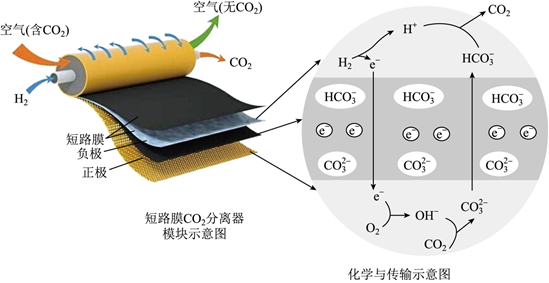
通过化学的方法实现CO2的资源化利用是一种理想的CO2减排途径。
Ⅰ.利用酸性水溶液电解池在铂电极上捕集CO2制储氢物质HCOOH
(1)CO2被 还原还原(填“氧化”或“还原”)为HCOOH,该铂电极为 阴阴极。
(2)写出该铂电极的电极方程式 CO2+2e-+2H+=HCOOHCO2+2e-+2H+=HCOOH。
(3)当电路中转移3mol电子时,理论上可生成HCOOH 6969g。
Ⅱ.利用CO2制备CO
一定温度下,在恒容密闭容器中投入一定量CO2和H2进行反应:CO2(g)+H2(g)⇌CO(g)+H2O(g)
(4)下列事实能说明上述反应达到平衡状态的是 CDCD(双选)
A.体系内n(CO):n(H2O)=1:1
B.体系压强不再发生变化
C.体系内各物质浓度不再发生变化
D.体系内CO的体积分数不再发生变化
(5)在恒定温度与容积下,可以提高CO2平衡转化率的措施有 ADAD(双选)
A.向反应容器中充入H2
B.向反应容器中充入CO2
C.添加更有效的催化剂
D.利用合适试剂干燥混合气体
(6)其他条件相同,在甲、乙、丙三种不同催化剂作用下,相同时间内测得氢气转化率随温度变化如图所示。下列说法错误的是 BB(单选)
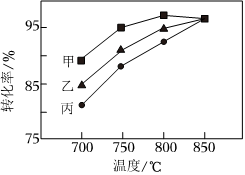
A.850℃下,该时间段内甲、乙、丙可能均达到平衡
B.700℃下,甲对应的活化能最大
C.一般催化剂既能降低活化能,又能降低过渡态的能量
D.其它条件一定时,随着温度升高,单位体积内活化分子数占比增大
Ⅲ.利用CO2制备甲醇
一定条件下,向恒容密闭容器中通入一定量的CO2和H2。涉及反应如下:
主反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)ΔH=−90.4kJ/mol
副反应:CO2(g)+H2(g)⇌CO(g)+H2O(g)ΔH=+40.5kJ/mol
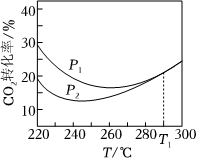
(7)其他条件相同,不同压强下,平衡时CO2转化率随温度的变化关系如图所示。
①压强P1>>P2(填“<”或“>”)。
②图2中温度高于T1时,两条曲线重叠的原因是:随着温度上升,主反应放热被抑制,副反应吸热被促进,T1温度后,体系中主要发生副反应,副反应是气体体积不变化的反应,压强改变对平衡没有影响,则两条曲线几乎交于一点随着温度上升,主反应放热被抑制,副反应吸热被促进,T1温度后,体系中主要发生副反应,副反应是气体体积不变化的反应,压强改变对平衡没有影响,则两条曲线几乎交于一点。
(8)实际工业生产中,需要在260℃、压强恒为4.0MPa的反应釜中进行上述反应。为确保反应的连续性,需向反应釜中以进气流量0.04mol/min、n(CO2):n(H2)=1:3,持续通入原料,同时控制出气流量。
①为了维持体系压强恒定,需控制出气流量小于进气流量,原因为:反应为气体分子数减小的反应,出气流速小才能保持反应釜内为压强恒定反应为气体分子数减小的反应,出气流速小才能保持反应釜内为压强恒定。
②已知出气流量为0.03mol/min,单位时间CO2的转化率为60%,则流出气体中CO的百分含量为 3.3%3.3%。
【答案】还原;阴;CO2+2e-+2H+=HCOOH;69;CD;AD;B;>;随着温度上升,主反应放热被抑制,副反应吸热被促进,T1温度后,体系中主要发生副反应,副反应是气体体积不变化的反应,压强改变对平衡没有影响,则两条曲线几乎交于一点;反应为气体分子数减小的反应,出气流速小才能保持反应釜内为压强恒定;3.3%
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/16 9:0:1组卷:26引用:1难度:0.5