铁及其化合物在日常生活生产中应用广泛,研究铁及其化合物的应用意义重大。回答下列问题:
(1)已知高炉炼铁过程中会发生如下反应:
FeO(s)+CO(g)=Fe(s)+CO2(g) ΔH1
Fe2O3(s)+13CO(g)=23Fe3O4(s)+13CO2(g) ΔH2
Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g) ΔH3
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH4
则ΔH4的表达式为ΔH4=ΔH2+23ΔH3ΔH2+23ΔH3(用含ΔH1、ΔH2、ΔH3的代数式表示)。
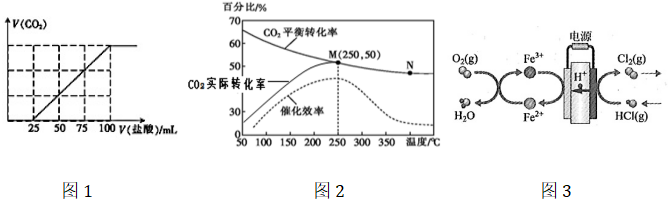
(2)把高炉出来的气体经过处理后通入NaOH溶液中完全吸收,再用0.01mol•L-1的盐酸溶液进行滴定,所得气体与滴入的盐酸体积的关系如图1,则滴定前溶液中离子浓度由大到小的顺序为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)。
(3)铁等金属可用作CO与氢气反应的催化剂。已知某种催化剂可用来催化反应CO(g)+3H2(g)⇌CH4(g)+H2O(g) ΔH<0。在T℃、106Pa时将1molCO和3molH2加入容积不变的密闭容器中,实验测得CO的体积分数φ(CO)如下表:
1
3
2
3
1
3
2
3
2
3
| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| φ(CO) | 0.25 | 0.23 | 0.214 | 0.202 | 0.200 | 0.200 |
ad
ad
(填字母)。a.容器内压强不再发生变化
b.混合气体的密度不再发生变化
c.v正(CO)=3v逆(H2)
d.混合气体的平均相对分子质量不再发生变化
②达到平衡时CO的转化率为
33.3%
33.3%
。③某种含铁催化剂可以催化合成乙烯:6H2(g)+2CO2(g)⇌CH2=CH2(g)+4H2O(g)。已知温度对CO2的平衡转化率、实际催化率和催化剂催化效率的影响如图2所示,结合图像分析温度低于250℃时CO2实际转化率变化的原因:
温度低于250℃时,随着温度升高,催化剂活性增强,反应速率加快,二氧化碳的实际转化率变大
温度低于250℃时,随着温度升高,催化剂活性增强,反应速率加快,二氧化碳的实际转化率变大
。(4)科学家最近采用碳基电极材料,在传统的电解氯化氢回收氯气技术的基础上,设计了一种新的工艺方案,主要包括电化学过程和化学过程,如图3所示.负极区发生的反应有Fe3++e−=Fe2+、
4Fe2++O2+4H+=4Fe3++2H2O
4Fe2++O2+4H+=4Fe3++2H2O
(写反应方程式)。【答案】ΔH2+ΔH3;c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+);ad;33.3%;温度低于250℃时,随着温度升高,催化剂活性增强,反应速率加快,二氧化碳的实际转化率变大;4Fe2++O2+4H+=4Fe3++2H2O
2
3
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/9/12 9:0:8组卷:21引用:3难度:0.7


