2022年北京冬季奥运会场馆使用了大量不锈钢材质,不锈钢属于合金钢,其基体是铁碳合金,常用的不锈钢中含铬(Cr)18%、含镍(Ni)8%。回答下列问题:
(1)碳的价电子层的电子排布式为 2s22p22s22p2;石墨烯(即单层石墨)是一种碳原子构成的单层二维蜂窝状晶格结构的新材料,其中碳原子采取 sp2sp2杂化。
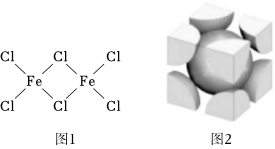
(2)铁的氯化物FeCl3蒸汽状态下以双聚分子形式存在(如图1),其中Fe的配位数为 44,双聚分子中存在配位键,提供空轨道的是 FeFe原子。
(3)甘氨酸亚铁[(H2NCH2COO)2Fe]中非金属元素的电负性由大到小的顺序是 O>N>C>HO>N>C>H。甘氨酸(H2NCH2COOH)比其同分异构体硝基乙烷(C2H5NO2)熔沸点高,其原因主要是 甘氨酸分子间能形成氢键甘氨酸分子间能形成氢键。
(4)FeCO3的阴离子的空间构型为 平面三角形平面三角形,写出一种与该阴离子互为等电子体的分子的化学式 BF3或SO3BF3或SO3。
(5)工业上常用羰基镍[Ni(CO)4]制备高纯镍,其熔点-19℃,沸点43℃,试分析晶体中σ键与π键数目的比值为 1:11:1,羰基镍属于 分子分子晶体。
(6)金属铬属于体心立方晶体(如图2),已知其密度为7.2g/cm3,阿伏加德罗常数的值为NA,则晶体中铬原子的半径为 34•352×27.2NA34•352×27.2NAcm(用含NA的表达式表示)。
3
4
•
3
52
×
2
7
.
2
N
A
3
4
•
3
52
×
2
7
.
2
N
A
【答案】2s22p2;sp2;4;Fe;O>N>C>H;甘氨酸分子间能形成氢键;平面三角形;BF3或SO3;1:1;分子;
3
4
•
3
52
×
2
7
.
2
N
A
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/8/31 2:0:8组卷:38引用:4难度:0.5
相似题
-
 1.铁及其化合物在生产生活及科学研究方面应用非常广泛。
1.铁及其化合物在生产生活及科学研究方面应用非常广泛。
(1)基态Fe原子的价层电子的电子排布图为;其最外层电子的电子云形状为。
(2)(NH4)2Fe(SO4)2•6H2O俗称摩尔盐
①NH4+电子式为。
②N、O两元素的第一电离能由大到小的顺序为(用元素符号表示)
③SO42-中S原子的杂化方式为,VSEPR模型名称为。
(3)K3[Fe(CN)6]晶体中中心原子的配位数为;晶体的配位体为(用化学符号表示)
(4)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为g•cm-3发布:2025/1/5 8:0:1组卷:7引用:1难度:0.7 -
 2.A、B、C、D、E、F是元素周期表中前四周期元素,且原子序数依次增大,其相关信息如下:
2.A、B、C、D、E、F是元素周期表中前四周期元素,且原子序数依次增大,其相关信息如下:
①A的周期序数等于其主族序数;
②B、D原子的L层中都有两个未成对电子;
③E元素原子最外层电子排布式为(n+1)Sn(n+1)Pn-1;
④F原子有四个能层,K、L、M全充满,最外层只有一个电子.
试回答下列问题:
(1)基态E原子中,电子占据的最高能层符号为,F的价层电子排布式为.
(2)B、C、D的电负性由大到小的顺序为(用元素符号填写),C与A形成的分子CA3的VSEPR模型为.
(3)B和D分别与A形成的化合物的稳定性:BA4小于A2D,原因是.
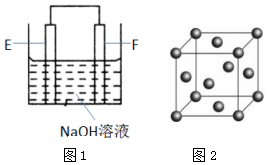
(4)以E、F的单质为电极,组成如图1所示的装置,E极的电极反应式为.
(5)向盛有F的硫酸盐FSO4的试管里逐滴加入氨水,首先出现蓝色沉淀,继续滴加氨水,蓝色沉淀溶解,得到深蓝色溶液,再向深蓝色透明溶液中加入乙醇,析出深蓝色晶体.蓝色沉淀溶解的离子方程式为.
(6)F的晶胞结构(面心立方)如图2所示:已知两个最近的F的距离为acm,F的密度为g/cm3(阿伏加德罗常数用NA表示,F的相对原子质量用M表示)发布:2025/1/18 8:0:1组卷:14引用:2难度:0.5 -
 3.碳及其化合物有着重要用途。回答下列问题:
3.碳及其化合物有着重要用途。回答下列问题:
(1)基态碳原子的价层电子排布图为。
(2)在CH2=CHCN中,碳原子的杂化方式有、,所含σ键数目和π键数目之比为。
(3)甲烷、水、氨气中C、O、N原子均采用sp3杂化方式,VSEPR模型均为正四面体构型,比较三者键角的大小(由大到小,用H一R-H表示),其原因是。
(4)C60室温下为紫红色固体,不溶于水,能溶于四氯化碳等非极性溶剂。据此判断C60的晶体类型是。
(5)C60晶胞结构如图,C60分子处于顶点和面心。已知:C60晶胞棱长为14.20Å (1Å=10-8cm),则C60的晶体密度为g/cm3。
C60体中存在正四面体空隙(例如1、3、6、7四点构成)和正八面体空隙(例如3、6、7、8、9、12六点构成),则平均每一个C60晶胞中有个正四面体空隙和4个正八面体空隙。当碱金属元素全部占满所有空隙后,这类C60掺杂物才具有超导性。若用金属铯(Cs)填满所有空隙,距离最近的两个Cs原子间的距离为Å。发布:2025/1/5 8:0:1组卷:53引用:2难度:0.4


