空气是一种重要的资源,人类的生产生活离不开空气,对于空气的研究人类从未停止。
研究一、从空气中获得氮气,进行氨气的合成
氨气是一种重要的化学物质,可用于制造硝酸和氮肥。工业合成氨气的流程如图1所示,在铁触媒作用下,用体积比为1:3的氮气和氢气合成氨气,当容器中氨的含量不再发生变化时(平衡时),测得氨气的含量分别与温度和压强的关系如图2所示。

(1)N2是合成氨气的重要原料。工业上可从空气中获得N2,该方法是利用空气中各成分的 沸点沸点不同将空气成分进行分离。
(2)从“合成塔”中出来的气体是 混合物混合物(填“纯净物”或“混合物”)。
(3)按下列条件进行合成氨气反应,平衡时氨气的含量最高的是 CC(填字母序号)。
A.200大气压、300℃
B.200大气压、500℃
C.400大气压、300℃
D.400大气压、500℃
研究二、三个实验小组同学分别利用不同的方法测定空气中氧气含量
A组实验:利用红磷燃烧测定空气中氧气含量
图3是利用气压传感器测定红磷燃烧时集气瓶内气压变化的实验装置;图4是集气瓶内气压的变化情况。
(4)用酒精灯点燃燃烧匙中过量的红磷。该反应的化学方程式是 4P+5O2 点燃 2P2O54P+5O2 点燃 2P2O5。
(5)点燃燃烧匙内的红磷后,立即伸入集气瓶中并把橡皮塞塞紧。待红磷熄灭并冷却后,打开止水夹。下列有关图4的分析不正确的是 DD。
A.BC段气压增大的主要原因是燃烧放热
B.CD段气压减小的主要原因是集气瓶内氧气不断被消耗且瓶内温度逐渐冷却
C.DE段气压增大的主要原因是烧杯中的水进入集气瓶
D.若用木炭代替红磷完成此实验,集气瓶内气压变化趋势与图4基本一致
(6)经多次实验发现,当反应停止并恢复至室温,用氧气浓度传感器测得集气瓶内始终有8%左右的氧气残留,但实际实验中倒吸入瓶内的水的体积能达到理论值(五分之一),其可能的操作原因是 点燃红磷伸入集气瓶太慢点燃红磷伸入集气瓶太慢。
B组实验:加热铜粉测定空气中氧气含量
图5是铜粉与氧气加热生成氧化铜实验装置:
(7)实验的主要实验步骤如下:
①组装装置,检查装置的气密性;
②向试管中加入足量的铜粉,铜粉要足量的原因是 消耗尽装置中的氧气消耗尽装置中的氧气;
③点燃酒精灯,不停地抽拉注射器的活塞,充分反应后停止加热。
(8)实验开始时,若注射器活塞前沿停在35mL的刻度线上,实验结束并等到具支试管冷却后观察,活塞前沿约停在 88mL的刻度线上。若实验过程中没有不断推拉注射器,则可能导致测定的氧气的体积分数 偏小偏小(填“偏大”“偏小”“不变”)。
(9)装置中小气球的作用是 防止装置内压强骤增,冲开橡皮塞防止装置内压强骤增,冲开橡皮塞。
C组实验:用铁生锈原理测定空气中氧气含量
图6是利用铁粉生锈消耗空气中的氧气和水,测定空气中氧气含量实验,实验数据如表:
点燃
点燃
| 测量项目 | 实验前烧杯中水的体积 | 实验后烧杯中剩余水的体积 | 集气瓶和导管的容积 |
| 体积/mL | 80.0 | 49.0 | 150.0 |
20.7%
20.7%
(计算结果精确到0.1%),相比较A组实验,该方法测定结果更精确。【答案】沸点;混合物;C;4P+5O2 2P2O5;D;点燃红磷伸入集气瓶太慢;消耗尽装置中的氧气;8;偏小;防止装置内压强骤增,冲开橡皮塞;20.7%
点燃
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/9/2 11:0:11组卷:37引用:2难度:0.5
相似题
-
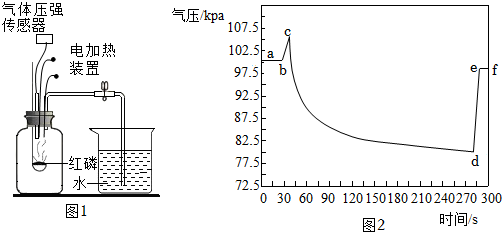
1.如图1是某化学兴趣小组利用气压传感器测定红磷燃烧时集气瓶内气压变化的实验装置。图2是集气瓶内气压随时间的变化情况。下列说法不正确的是( )
 发布:2024/12/25 11:30:2组卷:1085引用:3难度:0.7
发布:2024/12/25 11:30:2组卷:1085引用:3难度:0.7 -
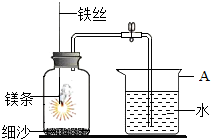 2.某校研究性学习小组用如图所示装置进行镁条在空气中燃烧的实验。待镁条完全燃烧并冷却后打开弹簧夹,进入集气瓶中水的体积约占集气瓶容积的70%。
2.某校研究性学习小组用如图所示装置进行镁条在空气中燃烧的实验。待镁条完全燃烧并冷却后打开弹簧夹,进入集气瓶中水的体积约占集气瓶容积的70%。
(1)图中A仪器的名称是。镁条燃烧并冷却后打开弹簧夹,水能进入到集气瓶中的原因是。
(2)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的%.现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中有氮气。
【发现问题】氮气是如何减少的?
【做出猜想】。
【查阅资料】镁条在氮气中能燃烧,产物为氮化镁(Mg3N2)固体。氮化化镁中氮的化合价是。镁条还可以在二氧化碳气体中燃烧生成碳和氧化镁,反应的化学方程式为2Mg+CO2C+2MgO,该反应所的基本反应类型是点燃。
(3)通过以上探究,你对燃烧的有关知识有了哪些新的认识?(写出一条即可)
(4)24g镁在二氧化碳中燃烧可生成多少克氧化镁?发布:2024/11/18 8:0:1组卷:13引用:1难度:0.5 -
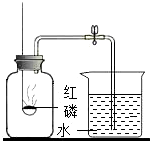 3.测定空气里氧气的含量,甲、乙、丙三个同学用如图所示的装置分别进行了实验探究。
3.测定空气里氧气的含量,甲、乙、丙三个同学用如图所示的装置分别进行了实验探究。
(1)实验时,取下橡胶塞,点燃红磷后迅速伸入集气瓶中并旋紧橡胶塞,这时看到的现象是,该反应的文字表达式为。
(2)甲同学:用足量的木炭代替红磷做测定空气中氧气含量的实验,结果实验失败了,请你帮助他分析失败的原因:。
(3)乙同学:想用镁条来代替红磷做实验,老师告诉他这种方法不是较好的方法,因为镁条在空气中燃烧非常剧烈,镁既可以和氧气反应,也可以和氮气反应生成氮化镁。请写出镁和氮气反应生成氮化镁的文字表达式:。
(4)丙同学:打算用铁丝替代红磷,实验能否成功?请说明理由。。
(5)燃烧后,集气瓶内剩余的气体主要是氮气,请结合本实验推测氮气的物理性质是。发布:2024/11/7 8:0:2组卷:19引用:1难度:0.5


