亚氯酸钠是一种高效氧化剂、漂白剂,主要用于棉纺、亚麻、纸浆漂白以及食品消毒、水处理、杀菌灭藻和鱼药制造。某校化学实验探究小组设计如图实验,用ClO2为原料制备亚氯酸钠(NaClO2)。
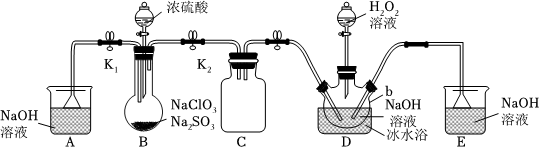
已知:
①2NaClO3+Na2SO3+H2SO4═2ClO2↑+2Na2SO4+H2O
②饱和NaClO2溶液中析出的晶体成分与温度的关系如表所示:
| 温度/℃ | <38 | 38~60 | >60 |
| 晶体成分 | NaClO2•3H2O | NaClO2 | NaClO2分解成NaClO3和NaCl |
(1)漂白剂有多种类型,从漂白原理来看,与亚氯酸钠均属于同类型的漂白剂有
D
D
(单选)。A.SO2、HClO
B.活性炭、H2O2
C.漂白粉、SO2
D.HClO、H2O2
(2)B中使用浓硫酸而不用稀硫酸的原因是
稀硫酸含水多,而ClO2极易溶于水,不利于ClO2逸出
稀硫酸含水多,而ClO2极易溶于水,不利于ClO2逸出
。(3)B中发生的反应,氧化剂与还原剂物质的量之比为
2:1
2:1
。(4)装置D中生成NaClO2的离子方程式为
2ClO2+2OH-+H2O2=2+2H2O+O2↑
C
l
O
-
2
2ClO2+2OH-+H2O2=2+2H2O+O2↑
。C
l
O
-
2
(5)装置D溶液采用结晶法提取NaClO2晶体,控制温度为
38~60
38~60
℃(填写范围)减压蒸发结晶,趁热过滤,50℃左右热水洗涤,低于60℃条件下干燥,得到成品。如果干燥温度过高可能导致产品中混有的杂质是 NaClO3和NaCl
NaClO3和NaCl
。测定样品中NaClO2的纯度。测定时进行如下实验:准确称取所得NaClO2样品mg于小烧杯中,加入适量蒸馏水和过量的碘化钾晶体,在酸性条件下发生充分反应:
C
l
O
-
2
+
4
I
-
+
4
H
+
=
2
H
2
O
+
2
I
2
+
C
l
O
2
-
3
O
2
-
6
(6)滴定终点的现象是
当滴入最后半滴Na2S2O3标准液时,溶液有蓝色变为无色,且半分钟内不恢复
当滴入最后半滴Na2S2O3标准液时,溶液有蓝色变为无色,且半分钟内不恢复
。(7)该样品中NaClO2质量分数为
9
.
05
c
V
m
9
.
05
c
V
m
【考点】制备实验方案的设计;探究物质的组成或测量物质的含量.
【答案】D;稀硫酸含水多,而ClO2极易溶于水,不利于ClO2逸出;2:1;2ClO2+2OH-+H2O2=2+2H2O+O2↑;38~60;NaClO3和NaCl;当滴入最后半滴Na2S2O3标准液时,溶液有蓝色变为无色,且半分钟内不恢复;%
C
l
O
-
2
9
.
05
c
V
m
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/9/9 0:0:8组卷:13引用:1难度:0.6
相似题
-
1.硫铁矿烧渣是硫铁矿生产硫酸过程中产生的工业废渣(主要含Fe2O3及少量SiO2、Al2O3、CaO、MgO等杂质).用该烧渣制取药用辅料--红氧化铁的工艺流程如图:
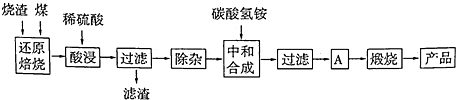
(1)在“还原焙烧”中产生的有毒气体可能有.
(2)“酸浸”时间一般不超过20min,若在空气中酸浸时间过长,溶液中Fe2+含量将下降,其原因是(用离子方程式表示).
(3)根据下表数据:
在“除杂”步骤中,为除去Fe3+和Al3+,溶液的pH最大值应小于氢氧化物 Al(OH)3 Mg(OH)2 Fe(OH)3 Fe(OH)2 开始沉淀的pH 3.10 8.54 2.01 7.11 完全沉淀的pH 4.77 11.04 3.68 9.61 ,检验Fe3+已经除尽的试剂是;当pH=5时,溶液中c(Al3+)=mol•L-1(已知常温下Ksp[Al(OH)3]=2.0×10-33).
(4)“中和合成”的目的是将溶液中Fe2+转变为碳酸亚铁沉淀,则A的操作是.
(5)a g烧渣经过上述工艺可得红氧化铁b g.药典标准规定,制得的红氧化铁中含氧化铁不得少于98.0%,则所选用的烧渣中铁的质量分数应不低于(用含a、b的表达式表示).发布:2025/1/19 8:0:1组卷:114引用:4难度:0.5 -
2.硫铁矿烧渣是硫铁矿生产硫酸过程中产生的工业废渣(主要含Fe2O3及少量SiO2、Al2O3等杂质).用该烧渣制取药用辅料--红氧化铁的工艺流程如下:
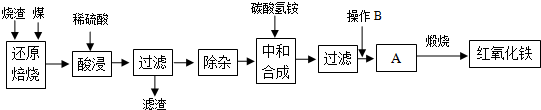
(1)在“还原焙烧”中产生的有毒气体可能有.
(2)“酸浸”时间一般不超过20min,若在空气中酸浸时间过长,溶液中Fe2+含量将下降,其原因是(用离子方程式表示).
(3)根据下表数据:
在“除杂”步骤中,为除去Fe3+和Al3+,溶液的pH最大值应小于氢氧化物 Al(OH)3 Fe(OH)3 Fe(OH)2 开始沉淀的pH 3.10 2.01 7.11 完全沉淀的pH 4.77 3.68 9.61 ,检验
Fe3+已经除尽的试剂是.
(4)“中和合成”的目的是将溶液中Fe2+转变为碳酸亚铁沉淀,则操作B是.
(5)煅烧A的反应方程式是.
(6)a g烧渣经过上述工艺可得红氧化铁b g.药典标准规定,制得的红氧化铁中含氧化铁不得少于98.0%,则所选用的烧渣中铁的质量分数应不低于(用含a、b的表达式表示).发布:2025/1/19 8:0:1组卷:5引用:1难度:0.5 -
3.硫铁矿烧渣是硫铁矿生产硫酸过程中产生的工业废渣(主要含Fe2O3及少量SiO2、Al2O3、CaO、MgO等杂质).用该烧渣制取药用辅料--红氧化铁的工艺流程如下:
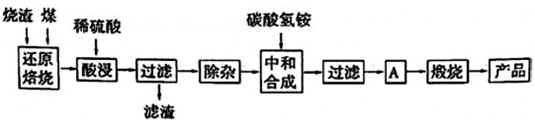
(1)在“还原焙烧”中产生的有毒气体可能有.
(2)“酸浸”时间一般不超过20min,若在空气中酸浸时间过长,溶液中Fe2+含量将下降,其原因是(用离子方程式表示).
(3)根据下表数据:
在“除杂”步骤中,为除去Fe3+和Al3+,溶液的pH最大值应小于氢氧化物 Al(OH)3 Mg(OH)2 Fe(OH)3 Fe(OH)2 开始沉淀的pH 3.10 8.54 2.01 7.11 完全沉淀的pH 4.77 11.04 3.68 9.61 ,常温下,当pH=5时,溶液中c(Al3+)=mol•L-1(已知常温下Ksp[Al(OH)3]═2.0×10-33).
(4)“中和合成”的目的是将溶液中Fe2+转变为碳酸亚铁沉淀,则A的操作是.发布:2025/1/19 8:0:1组卷:12引用:1难度:0.5


